Toán CO2 phản ứng với Kiềm quá cute khiến HS thương nhớ!
CO2 gặp NaOH, KOH, Ca(OH)2, Ba(OH)2 sẽ phản ứng loạn xạ. Con người với trí tưởng tượng phong phú; chế toán CO2 cute làm thí sinh thương nhớ.

Toán CO2 phản ứng với kiềm tuy dễ thương nhưng rất chảnh chẹ, bạn nào lơ mơ, lơ đễnh là nó bỏ đi liền. Hãy cẩn thận nha bạn.
Nội dung bài viết
1. Lập tỉ lệ kiểu truyền thống
1.1. Khi bé còn bé
Ở Hóa lớp 10 và 11; toán CO2 phản ứng với kiềm giải bằng cách lập tỉ lệ mol như sau:
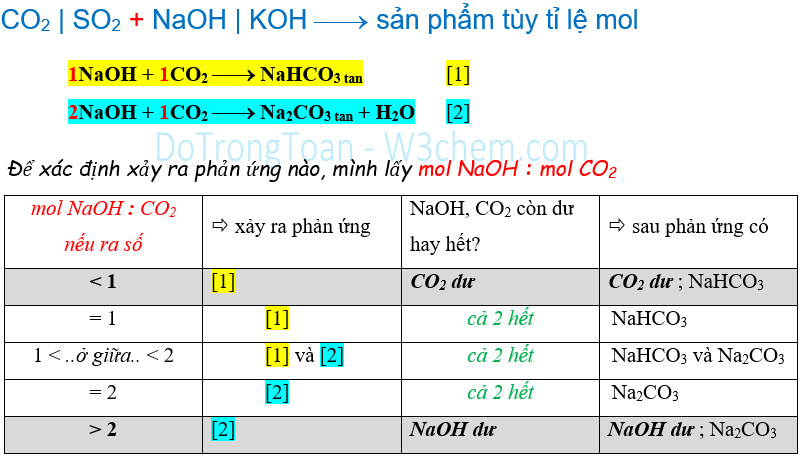
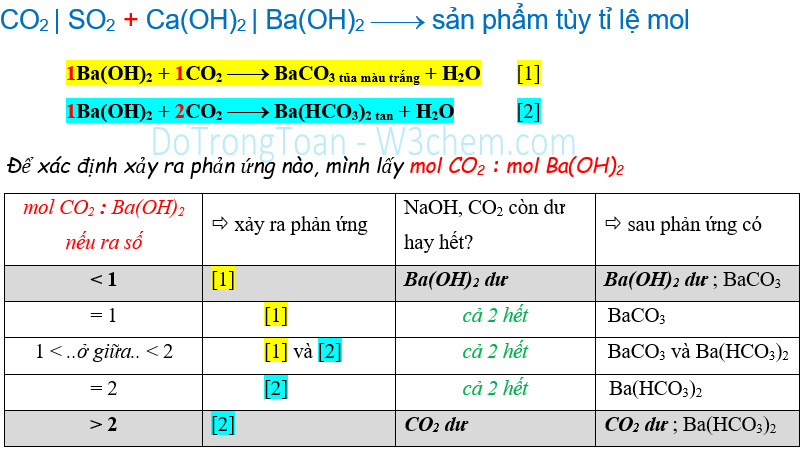
1.2. Khi bé lớn hơn
Ở Hóa lớp 12, toán CO2 phản ứng với kiềm sẽ nhìn công thức hai muối là biết lập tỉ lệ mol thế nào. Ví dụ:
Bài toán CO2 + NaOH → NaHCO3, Na2CO3 mình chỉ cần lập tỉ lệ dễ ợt là
- lấy mol Na : mol C
- sản phẩm và cách làm như trên, hãy tưởng tượng đôi chút nhe bạn
- hãy hỏi GV nếu cần
Bài toán CO2 + Ba(OH)2 → BaCO3, Ba(HCO3)2 mình chỉ cần lập tỉ lệ dễ ợt là
- lấy mol mol C : mol Ba
- sản phẩm và cách làm như trên, hãy tưởng tượng đôi chút nhe bạn
- hãy hỏi GV nếu cần
Tính toán cũng nhanh hơn, bằng cách dùng bảo toàn số mol nguyên tử C, Na, Ba. Hãy xem các bài tập đã giải bên dưới để hiểu hơn nha bạn.
1.2.1. Cho 100 gam CaCO3 tác dụng hoàn toàn với dung dịch HCl thu được khí CO2.
Dẫn lượng khí CO2 thu được vào dung dịch chứa 60 gam NaOH. Tính khối lượng muối tạo thành?
1 mol CaCO3 ⇒ 1 mol CO2 (bảo toàn mol nguyên tử C)
Có bài toán 1 mol CO2 + 1,5 mol NaOH
- tỉ lệ Na : C = 1,5 : 1 = 1,5 nên thu được hai muối NaHCO3 và Na2CO3
- đặt x mol NaHCO3 ; y mol Na2CO3
Bây giờ mình có hệ phương trình là
- nC = 1 ⇒ x + y = 1
- nNa = 1,5 ⇒ x + 2y = 1,5
- giải ra x = 0,5 và y = 0,5
Tính muối thu được
- mNaHCO3 = 84x = 42 gam
- mNa2CO3 = 106y = 53 gam
- tổng muối = 95 gam
1.2.2. Hấp thụ hoàn toàn 6,72 lít khí CO2 (đktc) vào dung dịch chứa a mol KOH,
thu được dung dịch chứa 33,8 gam hỗn hợp muối.Tìm a? (Thi CĐ 2014)
Có bài toán 0,3 mol CO2 + a mol KOH → 33,8 gam {x mol KHCO3 ; y mol K2CO3}
- nC = 0,3 ⇒ x + y = 0,3
- mmuối = 33,8 ⇒ 100x + 138y = 33,8
- giải ra x = 0,2 và y = 0,1
Vậy a = x + 2y = 0,4
2. Lập tỉ lệ từ phương trình ion
Như vậy tùy kiềm phản ứng, mà chúng mình phải lập tỉ lệ khác nhau, ví dụ NaOH : CO2 nhưng lúc khác lại là CO2 : Ca(OH)2. Điều này thật bất tiện, vì có đôi khi mình mơ mộng nên lơ đãng, lập tỉ lệ sai, làm kết quả sai theo.
Để thuận tiện hơn, người ta dùng phương trình ion và lập tỉ lệ như sau:

Điều này có nghĩa: cho dù bạn gặp bài CO2 + NaOH hay bài CO2 + Ca(OH)2; thì luôn luôn lập tỉ lệ OH– : CO2. Dễ quá phải không bạn! Hãy xem các ví dụ đã giải dưới đây một cách háo hức nha.
Giải lại ví dụ 1.2.1 bên trên
2.1. Cho 100 gam CaCO3 tác dụng hoàn toàn với dung dịch HCl thu được khí CO2.
Dẫn lượng khí CO2 thu được vào dung dịch chứa 60 gam NaOH. Tính khối lượng muối tạo thành?
+ 1 mol CaCO3 ⇒ 1 mol CO2 (bảo toàn mol nguyên tử C)
+ tiếp bài toán 1 mol CO2 + 1,5 mol NaOH
- mol OH– : CO2 = 1,5 : 1 = 1,5 nên xảy ra 2 phản ứng tạo NaHCO3 và Na2CO3
- mol CO32- = OH– – CO2 = 1,5 – 1 = 0,5 ⇒ mol Na2CO3 = 0,5
- mol HCO3– = CO2 – CO32– = 1 – 0,5 = 0,5 ⇒ mol NaHCO3 = 0,5
3. Dùng công thức và Đồ thị
3.1. CO2 + 1 Kiềm
3.1.1. Cho CO2+ Ca(OH)2 | Ba(OH)2 → tủa CaCO3 | BaCO3 với mol Ca2+, Ba2+ > CaCO3, BaCO3
Ta có hai kết quả
- nCO2 min = nBaCO3
- nCO2 max = nOH- bđ – nBaCO3 = 2nBa(OH)2 bđ – nBaCO3
- CO2 đỉnh tạo nBaCO3 max = nBa(OH)2 bđ
*Hấp thụ hết V lít CO2 (đo ở đktc) vào dung dịch có 0,3 mol Ba(OH)2
thu được 0,1 mol kết tủa. Tính V?
0,3 mol Ba(OH)2 ⇒ nOH- = 0,3.2 = 0,6
Đề không hỏi min hay max nên ta có 2 kết quả như sau:
- nCO2 min = ntủa = 0,1 ⇒ VCO2 min = 2,24 lit
- nCO2 max = nOH- – ntủa = 0,6 – 0,1 = 0,5 ⇒ VCO2 max = 11,2 lit
3.1.2. Ngắm đồ thị huyền thoại → Tìm số và tính toán
***Cảnh báo: Nếu quá vớ vẩn với bạn, xin hãy bỏ qua nội dung này.
Sở dĩ có hai trị CO2 do
- khi CO2 min ứng với chỉ xảy ra 1 phản ứng
1CO2 + 1Ba(OH)2 dư → BaCO3 + H2O
- khi CO2 max ứng với xảy ra cả 2 phản ứng
[1] CO2 phản ứng từ từ với Ba(OH)2 tạo tủa BaCO3 cho đến max
1CO2 + 1Ba(OH)2 hết → BaCO3 max + H2O
[2] CO2 tiếp tục hòa tan 1 phần BaCO3
1CO2 + 1BaCO3 một phần + H2O → Ba(HCO3)2 tan
Bây giờ, thay vì dùng đoạn văn để cung cấp số liệu; các nhà Toán-Hóa mong ước Hóa trở nên bí ẩn – ly kì – rùng rợn, họ vẽ hình rồi bắt thí sinh nhìn vào đó, tự đi tìm các số liệu để giải bài. Hãy xem các bài đã giải dưới đây; bạn phải có lòng can đảm và sự si mê để tìm hiểu, nếu vẫn không thể – vui lòng hỏi Thầy cô nha bạn!
*Dẫn từ từ khí CO2 vào dung dịch Ca(OH)2 cho đến khi phản ứng kết thúc.
Kết quả thí nghiệm được thể hiện trên đồ thị bên dưới. Giá trị của x trong đồ thị là A. 0,2. | B. 0,3. | C. 0,4. | D. 0,5.
Đề chỉ cho phần vẽ màu đen; màu xanh và đỏ do mình vẽ thêm vào cho đẹp!
Dễ dàng ta thấy: vì hai chất phản ứng với tỉ lệ 1:1 nên đồ thị là hình tam giác đều á.
/ trục chạy lên vẽ pứ [1] tạo tủa
\ trục chạy xuống vẽ pứ [2] khi tủa tan dần
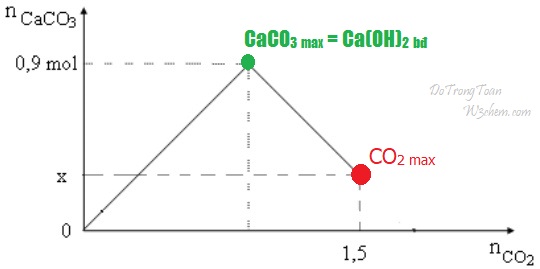
Ta dùng công thức chỗ CO2 max như sau
- nCO2 max = 2nCa(OH)2 bđ – nCaCO3 = 2.0,9 – x
- thế số được 1,5 = 2.0,9 – x ⇔ x = 0,3
***Một số bài còn giải theo kiểu hình học tam giác đều, bạn có hứng khởi thì tìm hiểu nha!
*Dẫn từ từ khí CO2 vào 400 gam dung dịch Ba(OH)2. Kết quả thí nghiệm khi
phản ứng kết thúc được biểu diễn trên đồ thị dưới đây. Dung dịch thu được có nồng độ phần trăm khối lượng là A. 42,46%. | B. 64,51%. | C. 50,64%. | D. 70,28%.
Đề chỉ cho phần vẽ màu đen; màu xanh và đỏ do mình vẽ thêm vào cho đẹp!
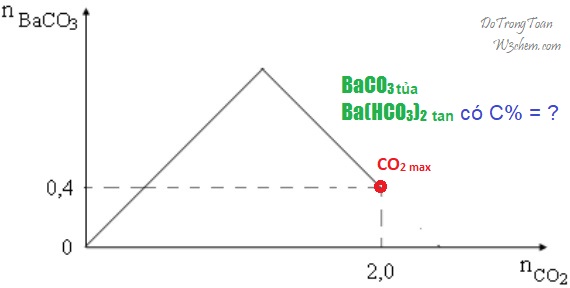
Dùng công thức và nhìn sơ đồ có
- CO2 max = 2Ba(OH)2 bđ – BaCO3
- thế số vào có 2 = 2Ba(OH)2 bđ – 0,4 ⇒ Ba(OH)2 bđ = 1,2
1,2 mol Ba(OH)2 ban đầu sau phản ứng chia ra
- BaCO3 tủa = 0,4
- nên Ba(HCO3)2 tan = 1,2 – 0,4 = 0,8 (do bảo toàn mol Ba)
Vậy
- chất tủa là BaCO3 có m = 197.0,4 = 78,8 gam
- chất tan là Ba(HCO3)2 có m = 259.0,8 = 207,2 gam
- mdd sau phản ứng = CO2 + dung dịch Ba(OH)2 – mBaCO3 tủa = 2.44 + 400 – 78,8 = 409.2 gam
- C% Ba(HCO3)2 = (207,2.100%) : 409,2 = 50,64
*Dẫn từ từ khí CO2 đến dư vào dung dịch Ba(OH)2, kết quả thí nghiệm
được thể hiện trên đồ thị dưới đây. Giá trị của a và x trong đồ thị lần lượt là A. 2 và 4. | B. 1,8 và 3,6. | C. 1,6 và 3,2. | D. 1,7 và 3,4.
Đề chỉ cho phần vẽ màu đen; màu xanh và đỏ do mình vẽ thêm vào cho đẹp!
/ trục chạy lên vẽ pứ [1] tạo tủa
\ trục chạy xuống vẽ pứ [2] khi tủa tan dần

Vì là tam giác đều nên x = 2a
- nCO2 max = nOH- bđ – nBaCO3 = 2nBa(OH)2 bđ – nBaCO3 = 2nBaCO3 max – nBaCO3
- thế số được 3 = 2.a – 0,5a ⇔ a = 2
Vậy x = 4
***Một số bài còn giải theo kiểu hình học tam giác đều, bạn có hứng khởi thì tìm hiểu nha!
*Dẫn từ từ đến dư khí CO2 vào dung dịch Ba(OH)2. Sự phụ thuộc của
khối lượng kết tủa (y gam) vào thể tích khí CO2 tham gia phản ứng (x lít) được biểu diễn bằng đồ thị bên dưới. Giá trị của m là A. 19,70. | B. 39,40. | C. 9,85. | D. 29,55. (Đề tham khảo 2019)
Đề chỉ cho phần vẽ màu đen; màu xanh và đỏ do mình vẽ thêm vào cho đẹp!
/ trục chạy lên là vẽ cho pứ [1]
\ trục chạy xuống là vẽ cho pứ [2]
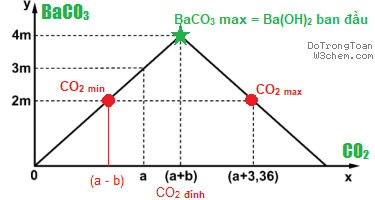
Có 3 ẩn a – b – m. Mình dùng công thức ở 3 chỗ đánh dấu tròn và ngôi sao là xong, dễ ẹt hà!
[1] CO2 min = BaCO3
- (a – b) : 22,4 = 2m : 197
- nên 197a – 197b – 44,8m = 0
[2] CO2 đỉnh = BaCO3 max
- (a + b) : 22,4 = 4m : 197
- nên 197a + 197b – 89,6m = 0
[3] CO2 max = 2Ba(OH)2 bđ – BaCO3
- (a + 3,36) : 22,4 = (2.4m : 197) – (2m : 197)
- nên 197a – 134,4m = – 661,92
Giả hệ ra a = 3,36 ; b = 1,12 ; m = 9,85
***Giang hồ còn giải theo kiểu hình học tam giác đều, tam giác vuông cân ..bla bla bla!
3.2. CO2 + nhiều kiềm
3.2.1. Cho CO2 + NaOH, Ba(OH)2, Ca(OH)2 → mol CaCO3, BaCO3
Khi có tỉ lệ mol 1 < OH– : CO2 < 2 ⇒ tạo HCO3– và CO32-, ta mới dùng được công thức
- mol CO32– = mol OH– – mol CO2
- đương nhiên mol HCO3– = CO2 – CO32– (bảo toàn mol C)
Và ta vẫn có các công thức sau:
- nCO2 min = nBaCO3 = nCO32-
- nCO2 max = tổng nOH- bđ – nBaCO3 = tổng nOH- bđ – nCO32-
*Chỉ cho 1 dung dịch Ba(OH)2 hoặc Ca(OH)2 thì mol CO32- = mol tủa
Ví dụ. Hấp thụ hết 0,5 mol CO2 (đktc) vào dung dịch có 0,35 mol Ba(OH)2. Tính khối lượng kết tủa thu được.
0,35 mol Ba(OH)2 ⇒ nBa2+ = 0,35 ; nOH– = 0,35.2 = 0,7
Vì tỉ lệ mol OH– : CO2 = 0,7 : 0,5 = 1,4 nên
- mol CO32– = mol OH– – mol CO2 = 0,2 = ntủa BaCO3
- nBaCO3 = 0,2.197 = 39,4 gam
*Nếu cho dung dịch chứa nhiều kiềm như NaOH, Ba(OH)2 hoặc Ca(OH)2 thì
- so sánh mol CO32- với Ba2+ | Ca2+ để tính ra mol tủa
- vì CO32- + Ba2+ (Ca2+) → CaCO3 (BaCO3)
Ví dụ. Hấp thụ hết 0,3 mol CO2 (đo ở đktc) vào dung dịch hỗn hợp gồm 0,03 mol NaOH và 0,18 mol Ba(OH)2. Tính khối lượng kết tủa thu được?
Tổng nOH- = 0,39 mol
Vì tỉ lệ mol OH̶ : CO2 = 0,39 : 0,3 = 1,3 nên
- mol CO32– = mol OH– – mol CO2 = 0,39 – 0,3 = 0,09
- phản ứng Ba2+ + CO32- → BaCO3
- mà Ba2+ = 0,18 > CO32- = 0,09 ⇒ nBaCO3 = 0,09 mol ~ 17,73 gam
3.2.2. Ngắm đồ thị huyền thoại → Tìm số và tính toán
***Cảnh báo: Nếu quá vớ vẩn với bạn, xin hãy bỏ qua nội dung này.
*Dẫn khí CO2 vào V lít dung dịch hỗn hợp NaOH 0,2 M và Ba(OH)2 0,1M.
Đồ thị biểu diễn khối lượng kết tủa theo số mol CO2 như dưới. Giá trị của V là A. 300. | B. 250. | C. 400. | D. 150. (THPTQG 2016)
Đề chỉ cho phần vẽ màu đen; màu xanh và đỏ do mình tô thêm vào cho đẹp!
/ là đường tạo BaCO3 tủa
— là đường tạo NaHCO3 tan
\ là đường BaCO3 tủa tan thành Ba(HCO3)2

Tổng nOH- bđ = 0,2.V + 0,1.V.2 = 0,4V
Và ta dùng các công thức như trên.
- nCO2 min = nBaCO3 = 0,03
- nCO2 max = tổng nOH- bđ – nBaCO3 ⇒ 0,13 = tổng nOH- bđ – 0,03 ⇔ tổng nOH- bđ = 0,16
Vậy 0,4V = 0,16 ⇔ V = 0,4 lit
Liên kết nhanh
Mời bạn vui thưởng thức thêm các bài viết khác của
Viết bởi Đỗ Trọng Toan từ W3chem.com
Mình là người tự thực hiện toàn bộ dự án này – bao gồm xây dựng trang web, viết nội dung, tìm tài liệu tham khảo, trả lời câu hỏi bạn gởi về. Vui lòng xem xét QUYÊN GÓP để hỗ trợ W3chem CHỈ BẰNG CÁCH CHIA SẺ BÀI VIẾT NÀY LÊN MẠNG XÃ HỘI; bởi vì trong tương lai, bạn sẽ cho mình nhiều thời gian để làm việc trên W3chem, cũng có nghĩa bạn nhận thêm nhiều nội dung mới nhanh hơn tại đây.😍 🥰 😘







Web của thầy hữu ích quá ạ! TL dể hiểu lắm lun.
Chào CHLHOA.
Cám ơn CHLHOA rất nhiều nha. Mong gặp lại CHLHOA ở những bài viết khác.
Chúc CHLHOA sức khỏe và hạnh phúc.
Trân trọng.