Điện phân nóng chảy, Điện phân dung dịch

Điện phân (Electrolysis) rất hay và vui!!! nhưng dễ bị lú lẫn sau khi học. Hãy cùng trải nghiệm xem có đúng không bạn nhe …he …he …he.
Nội dung bài viết
1. Điện phân là gì vậy?
1.1. Ước ao chinh phục phản ứng oxi hóa-khử
Kim loại Na phản ứng rất mãnh liệt với khí Clo, phương trình hóa học của phản ứng như sau:
2Na0 + Cl20 → 2Na+Cl–
Đây là một phản ứng oxi hóa khử do có sự đổi thay số oxi hóa của Na và Cl. Muối NaCl là hợp chất ion rất bền vững, tồn tại rất nhiều trong nước biển. Con người đã khai thác NaCl từ biển để ăn cho đã!
Bây giờ con người ao ước thực hiện được phản ứng ngược lại; để sản xuất được kim loại Na, khí Clo nhằm phục vụ cho nhiều mục đích; tức thực hiện phản ứng:
2Na+Cl– → 2Na0 + Cl20
Đây cũng là phản ứng oxi hóa khử; nhưng vấn đề là phản ứng này không thể xảy ra với các quá trình hóa học thông thường ⇒ phải thúc ép cho phản ứng xảy ra ⇒ nghiên cứu ra phản ứng điện phân.
1.2. Định nghĩa sự điện phân
1.2.1. Sự điện phân là gì?
Điện phân cũng chỉ là phản ứng oxi hóa-khử, nhưng xảy ra không phải cho chất oxi hóa + chất khử; mà xảy ra trên bề mặt điện cực (+) và điện cực (-) khi cho dòng điện 1 chiều chạy qua chất điện li (ở trạng thái nóng chảy hoặc trạng thái dung dịch nước). Điều đó có nghĩa là
- khác phản ứng oxi hóa-khử bình thường; con người phải dùng điện năng để thúc ép phản ứng xảy ra.
- chất khử không cho electron trực tiếp qua chất oxi hóa; mà chất khử truyền electron qua dây dẫn để đến chất oxi hóa.
1.2.2. Áp dòng điện 1 chiều vào chất điện ly
Khi cho dòng điện 1 chiều chạy qua chất điện ly nóng chảy; hoặc dung dịch chất điện ly thì
- các ion thôi không chuyển động hỗn loạn nữa;
- các ion chuyển động có hướng xác định như hình dưới đây:

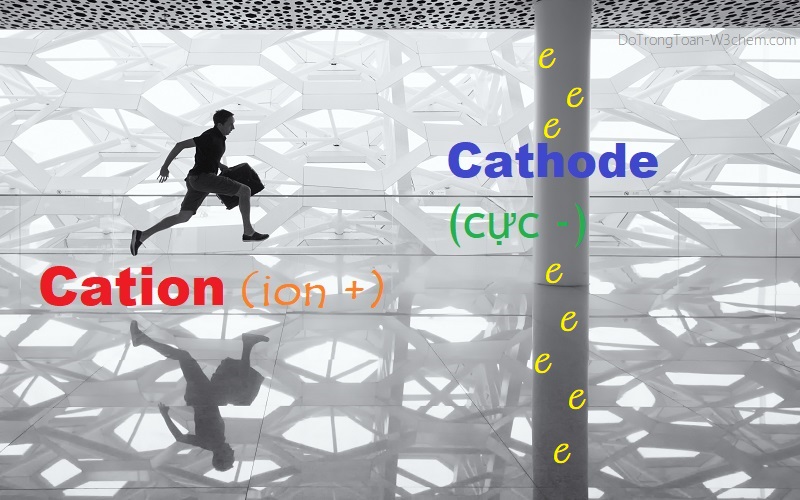
1.2.3. Chuyện gì xảy ra ở hai điện cực?
Hai quá trình sẽ xảy ra ở điện cực như bảng sau. Bạn xem phần Bình điện phân (Phần Pin điện hóa và Ăn mòn điện hóa là ở câu chuyện khác).

2. Điện phân nóng chảy
2.1. Mục đích
Để điều chế kim loại mạnh nhóm IA, IIA và Nhôm, trong đó
- Nhóm IA: điện phân nóng chảy muối clorua, bromua, hiđroxit.
- Nhóm IIA: điện phân nóng chảy muối clorua.
- Kim loại Al: điện phân nóng chảy oxit Al2O3 trong criolit.
2.2. Nguyên tắc
[1] Cation (ion +) chạy về Catot (cực -) ⇒ và Cation nhận e (chất oxi hoá ⇔ chất bị khử, sự khử)
- (Li+ Na+ K+ Rb+) + 1e → kim loại Li Na K Rb
- (Be2+ Mg2+ Ca2+ Sr2+ Ba2+) + 2e → kim loại Be Mg Ca Sr Ba
- Al3+ + 3e → kim loại Al
[2] Anion (ion -) chạy về Anot (cực +) ⇒ và Anion cho e (chất khử ⇔ chất bị oxi hoá, sự oxi hoá)
- 2Cl– → Cl2 + 2e
- 2Br– → Br2 + 2e
- 2O2- → O2 + 4e
- 4OH– → O2 + 2H2O + 4e [*]
2.3. Viết phương trình điện phân nóng chảy
Em hãy viết phương trình điện phân nóng chảy của: NaCl, MgCl2, Al2O3, NaOH?
2.3.1. Điện phân nóng chảy NaCl
+Khi NaCl nóng-chảy lỏng ra thì
- NaCl = [Na+ chạy về catot] [Cl– chạy về anot]
- [Na+][Cl–] —đpnc→ …?…
+Bây giờ mình nhìn lý thuyết trên sẽ thấy:
- Ở catot: Na+ → Na0
- Ở anot: Cl– → Cl2
- mình viết: NaCl —đpnc→ Na + Cl2
- cân bằng được 2NaCl —đpnc→ 2Na + Cl2
2.3.2. Điện phân nóng chảy MgCl2
+Khi MgCl2 nóng-chảy lỏng ra thì
- MgCl2 = [Mg2+ chạy về catot] [Cl– chạy về anot]
- [Mg2+][Cl–]2 —đpnc→ …?…
+Bây giờ mình nhìn lý thuyết trên sẽ thấy:
- Ở catot: Mg2+ → Mg0
- Ở anot: Cl– → Cl2
- mình viết: MgCl2 —đpnc→ Mg + Cl2
- phản ứng đã cân bằng, nên MgCl2 —đpnc→ Mg + Cl2
2.3.3. Điện phân nóng chảy Al2O3
+Khi Al2O3 nóng-chảy lỏng ra thì
- Al2O3 = [Al3+ chạy về catot] [O2- chạy về anot]
- [Al3+]2[O2-]3 —đpnc→ …?…
+Bây giờ mình nhìn lý thuyết trên sẽ thấy:
- Ở catot: Al3+ → Al0
- Ở anot: O2- → O2
- mình viết: Al2O3 —đpnc→ Al + O2
- cân bằng được Al2O3 → 2Al + 3/2O2
- hoặc quy đồng cho đẹp là 2Al2O3 —đpnc→ 4Al + 3O2
2.3.4. Điện phân nóng chảy NaOH
+Khi NaOH nóng-chảy lỏng ra thì
- NaOH = [Na+ chạy về catot] [OH– chạy về anot]
- [Na+][OH–] —đpnc→ …?…
+Bây giờ mình nhìn lý thuyết trên sẽ thấy:
- Ở catot: Na+ → Na0
- Ở anot: OH– → O2 + H2O
- mình viết: NaOH —đpnc→ Na + O2 + H2O
- cân bằng được 4NaOH —đpnc→ 4Na + O2 + 2H2O
+Những ưu tư
- Làm sao để sau phản ứng, Na hổng phản ứng với O2 ; với H2O?
- Phương trình này có được dùng trong thực tiễn để sản xuất Na, O2 không?
3. Điện phân dung dịch với điện cực trơ
Điện cực trơ là điện cực cứ trơ trơ ra (như nước đổ đầu vịt vậy đó!); có nghĩa nó hoàn toàn không tham gia ghì vào phản ứng oxi hóa khử đang xảy ra, cũng có nghĩa ta không cần quan tâm thì đến loại điện cực này.
3.1. Mục đích
Để điều chế kim loại trung bình – yếu và một số đơn chất phi kim.
Trong điện phân dung dịch, cũng xảy ra các quá trình cho-nhận electron như trên; nhưng do có H2O nên có thêm SỰ CẠNH TRANH CHO, NHẬN ELECTRON CỦA H2O.
- H2O là chất nhận e (chất oxi hóa): 2H2O + 2e → H2 + 2OH– [**]
- H2O là chất cho e (chất khử): 2H2O → O2 + 4H+ + 4e [***]
3.2. Nguyên tắc
[1] Cation chạy về Catot và

Ví dụ (bài chế, không biết có không?): điện phân dung dịch chứa các ion Na+, Ag+, Fe3+, Cu2+, H+, Pb2+; thứ tự nhận electron là
- Ag+ + 1e → Ag
- Fe3+ + 1e → Fe2+
- Cu2+ + 2e → Cu
- 2H+ + 2e → H2
- Pb2+ + 2e → Pb
- Fe2+ + 2e → Fe
- Khi các ion trên đã bị điện phân hết, chỉ còn Na+; mà
- Na+ không bị điện phân
- nên H2O sẽ tiếp tục điện phân theo phương trình [**]
[2] Anion chạy về Anot và
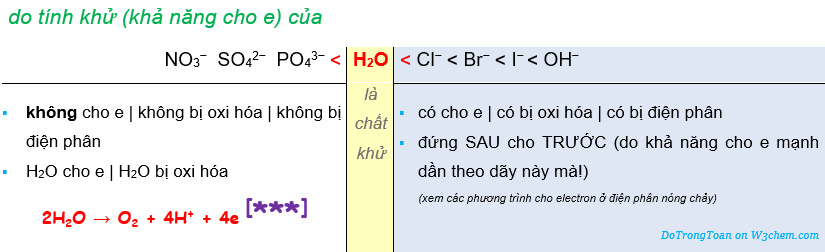
3.3. Viết phương trình điện phân dung dịch
Viết phương trình điện phân mỗi dung dịch (điện cực trơ) sau: CuSO4, Cu(NO3)2, AgNO3, NaCl?
3.3.1. Điện phân dung dịch CuSO4
+Dung dịch CuSO4 có
- H2O
- CuSO4 = [Cu2+ chạy về catot] [SO42- chạy về anot]
- [Cu2+][SO42-] + H2O —đpdd→ …?…
+Khi cho dòng điện 1 chiều chạy qua dung dịch, nhìn lý thuyết trên thấy:
- Ở catot: Cu2+ → Cu0
- Ở anot: SO42- —x→ SO42- ; nên H2O → O2 + H+
- Mình viết: CuSO4 + H2O —đpdd→ Cu + SO42- + O2 + H+
+Gom SO42- với H+ thành H2SO4, lúc này có
- CuSO4 + H2O → Cu + H2SO4 + O2
- cân bằng được CuSO4 + H2O → Cu + H2SO4 + 1/2O2
- hoặc qui đồng cho đẹp là 2CuSO4 + 2H2O → 2Cu + 2H2SO4 + O2
3.3.2. Điện phân dung dịch Cu(NO3)2
+Dung dịch Cu(NO3)2 có
- H2O
- Cu(NO3)2 = [Cu2+ chạy về catot] [NO3– chạy về anot]
- [Cu2+] [NO3–]2 + H2O —đpdd→ …?…
+Bây giờ nhìn lý thuyết trên, em thấy:
- Ở catot: Cu2+ → Cu0
- Ở anot: NO3– —x→ NO3– ; nên H2O → O2 + H+
- Mình viết: Cu(NO3)2 + H2O —đpdd→ Cu + NO3– + O2 + H+
+Gom NO3– với H+ thành HNO3, lúc này có
- Cu(NO3)2 + H2O → Cu + HNO3 + O2
- cân bằng được Cu(NO3)2 + H2O → Cu + 2HNO3 + 1/2O2
- hoặc qui đồng cho đẹp là 2Cu(NO3)2 + 2H2O → 2Cu + 4HNO3 + O2
3.3.3. Điện phân dung dịch AgNO3
+Dung dịch AgNO3 có
- H2O
- AgNO3= [Ag+ chạy về catot] [NO3– chạy về anot]
- [Ag+][NO3–]+ H2O —đpdd→ …?…
+Bây giờ hãy nhìn lý thuyết, sẽ thấy:
- Ở catot: Ag+ → Ag0
- Ở anot: NO3– —x→ NO3– ; nên H2O → O2 + H+
- Mình viết: AgNO3 + H2O —đpdd→ Ag + NO3– + O2 + H+
+Gom NO3– với H+ thành HNO3, lúc này có
- AgNO3 + H2O → Ag + HNO3 + O2
- cân bằng được AgNO3+ H2O → Ag + HNO3 + 1/2O2
- hoặc qui đồng cho đẹp là 2AgNO3 + 2H2O → 2Ag + 2HNO3 + O2
3.3.4. Điện phân dung dịch NaCl
+Dung dịch NaCl có
- H2O
- NaCl = [Na+ chạy về catot] [Cl– chạy về anot]
- [Na+][Cl–]+ H2O —đpdd→ …?…
+Bây giờ khi nhúng 2 điện cực vào dung dịch NaCl; nhìn lý thuyết thấy:
- Ở catot: Na+ —x→ Na+ ; nên H2O → H2 + OH–
- Ở anot: Cl– → Cl2
- Mình viết: NaCl + H2O —đpdd→ Na+ + H2 + OH– + Cl2
+Gom Na+ với OH– thành NaOH, lúc này có
- NaCl + H2O → NaOH + H2 + Cl2
- cân bằng được NaCl + H2O → NaOH + 1/2H2 + 1/2Cl2
- hoặc qui đồng cho đẹp là 2NaCl + 2H2O → 2NaOH + H2 + Cl2
+Lưu ý:
- NaOH sẽ tiếp tục phản ứng với Cl2 tạo ra nước Javen (Hóa lớp 10)
2NaOH + Cl2 → NaCl + NaClO + H2O
- Muốn phản ứng tạo Javel không xảy ra, người ta phải dùng vách ngăn giữa hai điện cực; để NaOH không thể gặp được Cl2; khi đó phương trình viết đầy đủ là
2NaCl + 2H2O —đpdd có vách ngăn→ NaOH + H2 + Cl2
- Như vậy, từ phương trình điện phân dung dịch NaCl, con người sản xuất được 4 hóa chất luôn: NaOH, Cl2, H2, Nước Javel (khi bỏ vách ngăn ra).
3.4. Điện phân H2O
H2O điện phân theo phương trình:
2H2O —điện phân→ 2H2 + O2
Hồi nhỏ khi học lớp 11, mình đã biết H2O điện ly rất yếu ra H+ và OH–; có nghĩa H2O nguyên chất không dẫn điện luôn, nên không thể tiến hành điện phân H2O được (NHỚ muốn điện phân thì chất đó phải có tính dẫn điện để dòng điện mới chạy qua được).
Các nhà hóa học “vò đầu bức tai” và …đã tìm ra hóa chất pha vào H2O để sao cho:
- Dung dịch trở nên dẫn điện tốt hơn.
- Hóa chất đó không bị điện phân hoặc không bị tiêu hao; sao cho dung dịch luôn dẫn điện được.
- Sản phẩm của cả quá trình điện phân là phương trình 2H2O —điện phân→ 2H2 + O2
Dưới đây liệt kê các hóa chất pha vào H2O; dĩ nhiên bao gồm thực tế và ảo do bài tập chế từ các nhà toán hóa!
- Dung dịch loãng của axit mạnh H2SO4 HNO3 (?) HClO4 (?).
- Dung dịch bazơ mạnh LiOH NaOH KOH Ba(OH)2 Ca(OH)2 Sr(OH)2.
- Dung dịch muối nitrat NO3–, sunfat SO42- của ion kim loại mạnh Li+ Na+ K+ Ba2+ Ca2+ Sr2+.
Viết phương trình điện phân mỗi dung dịch (điện cực trơ) sau: NaNO3, NaOH, H2SO4 loãng?
***Cách viết phương trình điện phân sẽ khác trên để dễ hiểu trong các bài này.
3.4.1. Điện phân dung dịch NaNO3
Dung dịch NaNO3 có
- H2O
- NaNO3 = [Na+ chạy về catot] [NO3– chạy về anot]
- [Na+][NO3–]+ H2O —đpdd→ …?…
Bây giờ khi nhúng 2 điện cực vào dung dịch NaNO3; mình nhìn lý thuyết trên thấy:
- Ở catot: Na+ —x→ Na+ ; nên 2H2O + 2e → H2 + 2OH–
- Ở anot: NO3– –x→ NO3– ; nên 2H2O → O2 + 4H+ + 4e
Cân bằng số electron cho = số electron nhận, tức
- 4H2O + 4e → 2H2 + 4OH–
- 2H2O → O2 + 4H+ + 4e
Cộng hai vế được 6H2O + 4e → 2H2 + O2 + 4H2O + 4e
Rồi đơn giản H2O và 4e ở hai vế, được 2H2O → 2H2 + O2
3.4.2. Điện phân dung dịch NaOH
Dung dịch NaOH có
- H2O
- NaOH = [Na+ chạy về catot] [OH– chạy về anot]
- [Na+][OH–]+ H2O —đpdd→ …?…
Bây giờ khi nhúng 2 điện cực vào dung dịch NaOH; mình nhìn lý thuyết trên thấy:
- Ở catot: Na+ —x→ Na+ ; nên 2H2O + 2e → H2 + 2OH–
- Ở anot: 4OH– → O2 + 2H2O + 4e
Cân bằng số electron cho = số electron nhận, tức
- 4H2O + 4e → 2H2 + 4OH–
- 4OH– → O2 + 2H2O + 4e
Cộng hai vế được 4H2O + 4OH– + 4e → 2H2 + 4OH– + 2H2O + 4e
Rồi đơn giản OH– , 4e và H2O ta được 2H2O → 2H2 + O2
3.4.3. Điện phân dung dịch H2SO4
Dung dịch H2SO4 có
- H2O
- H2SO4 = [H+ chạy về catot] [SO22- chạy về anot]
- [H+]2[SO42-]+ H2O —đpdd→ …?…
Bây giờ khi nhúng 2 điện cực vào dung dịch H2SO4; mình nhìn lý thuyết trên thấy:
- Ở catot: 2H+ + 2e → H2
- Ở anot: SO42-—x→ SO42-; nên 2H2O → O2 + 4H+ + 4e
Cân bằng số electron cho = số electron nhận, tức
- 4H+ + 4e → 2H2
- 2H2O → O2 + 4H+ + 4e
Cộng hai vế được 4H+ + 4e + 2H2O → 2H2 + O2 + 4H+ + 4e
Rồi đơn giản H+ và 4e ở hai vế, ta được 2H2O → 2H2 + O2
4. Điện phân dung dịch với điện cực tan
Điện cực Anot sẽ tham gia vào phản ứng oxi hóa-khử nên (bị mòn) bị tan dần. Phương pháp này ứng dụng để mạ một lớp kim loại mỏng lên trên bề mặt một kim loại khác, hoặc để tinh chế kim loại quý như Vàng (Au).
Nhưng loại này khó nhai lắm; nên khi nào bạn vào chuyên ngành này thì sẽ tự nhai tốt thôi. Chúng mình bỏ qua cho đỡ vất vả nha.
Nếu bạn vẫn cương quyết, muốn học cho bằng được phần này; vui lòng đọc thêm về Mạ điện (Electroplating) tại đây (Cảnh báo: tài liệu toàn tiếng Anh; bấm chọn dịch tiếng Việt có thể sai lệch thuật ngữ chuyên môn. Bạn cần cân nhắc trước khi xem!).
5. So sánh Điện phân & Pin điện hóa (Ăn mòn điện hóa)
5.1. Trong pin điện hóa
- Phản ứng oxi hóa – khử tự xảy ra được. Sự di chuyển electron từ chất khử đến chất oxi hóa phát sinh dòng điện.
- Nói: hóa năng (năng lượng hóa học) từ phản ứng oxi hóa – khử đã chuyển thành điện năng.
5.2. Trong bình điện phân
- Phản ứng oxi hóa – khử không tự xảy ra được; mà con người phải dùng điện 1 chiều truyền vào 2 điện cực trong bình điện phân (chứa chất điện li) để thúc ép phản ứng xảy ra.
- Nói: dùng điện năng bên ngoài chuyển thành hóa năng thúc ép phản ứng oxi – khử phải xảy ra.
5.3. Vì sao tên điện cực tréo ngoe?
Đọc thêm về Ăn mòn điện hóa tại đây.
Nếu đọc kĩ rồi suy nghĩ các nội dung trên, bạn sẽ thấy cách thức xảy ra trong Pin điện hóa và Bình điện phân là NGƯỢC NHAU. Điều này dẫn đến tên điện cực tréo ngoe như sau:
| Tên điện cực | ANODE | CATHODE |
| Xảy ra | sự oxi hóa | sự khử |
| Pin điện hóa Ăn mòn điện hóa | CỰC – chất khử cho e | CỰC + chất oxi hóa nhận e |
| Điện phân | CỰC + của dòng điện khiến ion âm hoặc H2O phải cho e | CỰC – của dòng điện khiến ion dương hoặc H2O phải nhận e |
Nếu quá khó để hiểu, thì thôi …mình lướt qua phần này cho cuộc đời vui nhe bạn!
6. Liên kết nhanh
Đọc thêm các bài viết của Hóa lớp 12 tại đây.
Tác giả: Đỗ Trọng Toan từ W3chem.com
Mình là người tự mình thực hiện toàn bộ dự án này – bao gồm xây dựng trang web, viết nội dung, tìm tài liệu tham khảo, trả lời câu hỏi bạn gởi về. Vui lòng xem xét QUYÊN GÓP để hỗ trợ W3chem CHỈ BẰNG CÁCH CHIA SẺ BÀI VIẾT NÀY LÊN MẠNG XÃ HỘI; bởi vì trong tương lai, bạn sẽ cho mình nhiều thời gian để làm việc trên W3chem, cũng có nghĩa bạn có thể nhận thêm nhiều nội dung mới nhanh hơn tại đây. 😍 🥰 😘
Mình cảm ơn bạn rất nhiều ⤵








ad ơi cho e hỏi là trong quá trình điện phân cu(no3)2 phải có vách ngăn để tránh H+ qua bên catot kết hợp với ion NO3- tác dụng với Cu nhỉ
Câu hỏi rất hay; Tên người hỏi cũng hay luôn!!!
🎁 Trong bài ACID BASE LÀ CHẤT GÌ?, mình đọc kỹ sẽ biết rằng ION H+ LÀ HẠT PROTON. Mình đã biết hạt proton nằm trong hạt nhân nguyên tử; mà hạt nhân nguyên tử rất bé, vậy nên… kích thước hạt proton còn bé hơn rất nhiều (mình hỏi bác google sẽ thấy rất nhiều bài viết-nên đọc các bài của nước ngoài).
🤔 Vậy mình phải CHẾ RA 1 CÁI MÀNG NGĂN giống như 1 TẤM LƯỚI CÁ; nhưng KÍCH THƯỚC CỦA MỖI Ô phải BÉ HƠN KÍCH THƯỚC CỦA H+ (HẠT PROTON) để mà …H+ không thể nào chui tọt qua lỗ của tấm lưới đó để chạy đi chỗ khác! Mình có nghĩ điều này có khả thi không?
😓 Thật khó để con người tạo ra cái màng ngăn như thế; mà nếu có – sẽ mất rất nhiều tiền của để làm. Nếu làm ra được thì mình sẽ làm gì? Mục đích đưa vào sản xuất gì đó… thì người ta sẽ tìm cách khắc phục vừa đơn giản, vừa tiết kiệm phải không nào?
***ĐẶC BIỆT: ion H+ là BÉ NHẤT trong tất cả các ion; vậy nếu H+ không chui qua được, thì tất cả các ion còn lại đều bị MẮC KẸT ở hai bên, không thể di chuyểu qua lại. Điều này dẫn đến kết quả là QUÁ TRÌNH ĐIỆN PHÂN DỪNG LẠI LẬP TỨC. Vì muốn điện phân được thì dung dịch phải dẫn điện được – tức các ion phải di chuyển được giữa hai điện cực. Điện phân dừng lại thì bài toán kết thúc!!!!. Mình cũng suy nghĩ thêm: đến cả các phân tử H2O cũng bị kẹt mỗi bên điện cực luôn – hổng biết làm sao nữa?
📒 Trong chương trình, mình thấy câu ĐIỆN PHÂN DUNG DỊCH CÓ MÀNG NGĂN xuất hiện khi ĐIỆN PHÂN DUNG DỊCH NaCl nhằm NGĂN PHÂN TỬ KHÍ Cl2 CHẠY QUA GẶP NaOH – phản ứng tạo nước Javen!. Màng ngăn đây là được bởi vì phân tử khí Cl2 to bự, nên nó không thể chui tọt qua màng ngăn con người đã chế tạo được (màng ngăn này thế nào T cũng chưa bao giờ biết luôn. Mình phải hỏi thăm kĩ sư hóa chất trong nhà máy sản xuất mới hiểu được!).
🫑 Thường thấy Hóa ở VN chế thế này: Điện phân có màng ngăn dung dịch chứa Cu(NO3)2 và NaCl… Nếu vậy thì mục đích màng ngăn là cản Cl2 chạy tùm lum!, còn ion H+ thì thua, nó vẫn chạy và kết hợp với NO3- để tiếp tục phản ứng với Cu.
***Còn nếu thấy chế: Điện phân có màng ngăn dung dịch chứa Cu(NO3)2 thôi ; thì T hổng biết ý người ra đề là gì? Nếu mục đích màng ngăn để cản H+ thì có lẽ…. trí tưởng tưởng tuyệt vời.
***Lại nhắc lại, Hóa là môn Khoa học Tự nhiên, bất cứ gì mình dùng trí tưởng tượng của mình để áp đặt có thể sẽ không đúng thực tiễn. Chỉ dùng để đánh đố, chế các bài toán hóa cho nhức đầu thôi!
Bài viết và trả lời của thầy tâm huyết quá ạ! Em cảm ơn thầy ạ 🙂
Mến chào Ba Con Sâu Đo…
Nếu có thời giờ, em đọc thêm câu trả lời đầy đủ ở đây nha.
Rất cám ơn lời khen của em và… cám ơn cái tên “BA CON SÂU ĐO” 🐛🐛🐛 thật dân dã nhưng rất ấn tượng!…
Trân trọng.
đpdd cu(no3)2 có màng ngăn nha
màng ngăn ion no3- là đc còn h+ ko phản ứng cu
Rất cám ơn phần trả lời của bạn Wistuck.
Chúc bạn sức khỏe và thành đạt. Mong gặp bạn ở các nội dung khác.
Trân trọng,
Toan từ W3chem.con
Nhưng mà em cũng nghĩ là trong quá trình đang điện phân thì HNO3 không phản ứng với Cu. Mà trong các TH đề hỏi thì ý của họ là sản phẩm thu được ngay sau khi mới điện phân xong nên không cần xét TH HNO3 + Cu cũng được ạ
Bài viết của em làm T nhớ lại đề thi vào ĐH Y Dược Tp.HCM một năm nào đó cách đây đã rất lâu rồi… thời còn thi tự luận.
Một năm nào đó, đề thi ra với suy nghĩ của người chế đề: hoàn toàn hổng có phản ứng giữa Cu + HNO3.
Năm sau đó, để đề thi nguy hiểm hơn, người chế đề ra thêm dữ liệu” …để yên dung dịch sau điện phân một thời gian!!!!… Thế là biết bao nhiêu bé, thậm chí cả T và mấy bài giải tham khảo của GV cũng bị mắc bẫy người chế đề luôn – vẫn giải như cũ – tức hổng có phản ứng Cu + HNO3.
!!! Bởi vì ông ra đề đã nói …để yên đó cơ mà _ ý ổng muốn là chúng nó sẽ có thời gian để gặp gỡ phản ứng với nhau!!!
Đấy, không hiểu ý của người chế đề là khổ lắm đó.
Vấn đề ở đây là… chúng ta vẫn quen thói áp đặt những suy nghĩ-lập luận từ lý thuyết của mình vào thế giới của Tự nhiên; điều này đôi khi hoàn toàn không đúng. Đúng ra chúng mình phải dựa trên những thực nghiệm khoa học đã được chứng thực từ các nguồn uy tín để dạy_để ra đề cho chính xác tuân theo TỰ NHIÊN; chứ không phải là chế đề theo cảm quan, theo suy nghĩ.
Một kinh nghiệm thường gặp trong cuộc sống hay thậm chí trong gia đình mình;
Bố mẹ nhiều khi dùng kinh nghiệm, suy nghĩ của mình để muốn con A là người yêu của mình, vì nó đẹp-giỏi-con nhà gia giáo..v.v… Thế mà mình cứ đâm đầu vào con B vì mình thấy quá tuyệt vời-không còn gì để chê luôn, hơn gấp bội con A.
Ba Con Sâu Đo thấy không? Bố mẹ suy nghĩ cho là quá đúng… nhưng vào thực nghiệm lại sai hoàn toàn.
Vậy chế đề theo suy tính của mình cũng nguy hiểm lắm. Chỉ làm khổ Học sinh và làm khổ cả mình (suy tính đong đo để ra đề lắc léo có khi hói cả đầu 👴).
Thôi vì đề thi hiện nay nó vậy, nên Ba Con Sâu Đo và các bạn chịu khó vậy!.
Trân trọng bài viết của em.
Mong gặp lại 🐛🐛🐛 ở các câu trả lời khác.
Thân!
Thầy ơi cho e hỏi. Cái này nó là thực tế đi làm e gặp phải. Bài toán đưa ra là tìm ra 1 dung dịch dẫn điện nhưng lại không bị điện phân. Sử dụng 2 điện cực là đồng và dòng điện xoay chiều? Dòng điện xoay chiều nó làm thay đổi điện cực liện tục có khi nào tần số quá nhanh nó làm cho điện cực ko kịp điện phân hay kiểu đảo ngược quá trình điện phân không? E sử dụng dòng điện 40v500hz?
Chào BaBy Chem (tên hay quá).
🍓Tìm một chất mà dung dịch của nó DẪN ĐIỆN được, nhưng KHÔNG BỊ ĐIỆN PHÂN thì dễ.
🌿Mình tìm chỗ các Cation (ion +) thấy các ion như Li+, K+, Ba2+, Ca2+, Na+, Mg2+, Al3+ không bị điện phân.
🌿Mình xem bên trên chỗ các Anion (ion -) thấy các ion như NO3-, SO42-, PO43- không bị điện phân.
Vậy mình kết hợp các ion trên lại với nhau sẽ tạo thành MUỐI [như NaNO3, K2SO4, Ba(NO3)2, …] điện ly được trong dung dịch nước; nhưng bản thân các ion đó hoàn toàn không điện phân gì cả… mà lúc này ở 2 điện cực, phân tử H2O sẽ bị điện phân [phương trình cuối cùng là 2H2O ➡︎ 2H2 + O2🌞].
🌿Mình cũng tiếp tục xem bên trên thấy khi điện phân dung dịch loãng của acid mạnh như H2SO4; base mạnh như NaOH thì cũng có phương trình điện phân H2O🌞 như trên. Trường hợp này ion H+ của acid, ion OH- của base có bị điện phân; nhưng nó được bù lại bởi ion H+,OH- do H2O khi bị điện phân sinh ra ở điện cực… và như vậy ion H+, OH- không đổi. Acid H2SO4, base NaOH nhằm tạo ra dung dịch dẫn điện để quá trình điện phân mới xảy ra được.
🌿Tất cả điều trên chỉ là lý thuyết GV dạy ở trường phổ thông thôi. T cũng hổng biết trong thực tế ở nhà máy, người ta dùng chất nào (vì nó còn liên quan đến kĩ thuật máy móc và nhiều vấn đề nữa). Cái này BaBy Chem nên hỏi thêm Giảng viên các trường ĐH liên quan đến kĩ thuật hóa học (như ĐH Bách Khoa) ; hoặc kĩ sư nhà máy sản xuất Hóa chất làm trong lãnh vực này thì rõ nhất.
🍓Câu hỏi phần sau khó quá, T chưa gặp kiểu này luôn (học từ Sư phạm ra chỉ toàn gặp các bài toán & lý thuyết ẢO không hà, có bao giờ biết trong thực tiễn thế nào đâu?.
Nó liên quan đến kĩ sư Hóa học chuyên làm việc trong nhà máy; hoặc phải gặp một Giảng viên ĐH nào đó có dạy phần này.
☘️T cũng tiếp tục lục lọi tìm hiểu trên mạng xem sao, hy vọng tìm được câu trả lời thỏa đáng nha BaBy Chem.
☘️Quý bạn đọc nếu có câu trả lời (bất kì nội dung nào), xin mời đóng góp vào phần comment này.
Rất cám ơn câu hỏi của BaBy Chem.
Trân trọng.