Đề tốt nghiệp THPT từ năm 2025 – Phần II có 4 câu hỏi Đúng – Sai
Đề thi tốt nghiệp THPT môn Hoá năm 2025 theo model mới; gồm 3 phần. Đây là Phần II, phần này có 4 câu, bạn suy nghĩ rồi tô vào ô Đúng hoặc Sai nha!.
😘 Đề tốt nghiệp THPT – Phần I (4,5 điểm) có 18 câu hỏi 4 lựa chọn A. B. C. D. xem tại đây nè!
🤗 Đề tốt nghiệp THPT – Phần III (1,5 điểm) có 6 câu hỏi Trả lời ngắn.
Đề tốt nghiệp THPT ở Phần II này, bé nhớ tô vào ô Đúng hoặc Sai thôi nha. Câu dễ làm ngay, câu khó đánh dấu để đó làm sau nhe.
Có 4 câu, chia như sau:
- 2 câu Lí thuyết gồm 1 Vô cơ – 1 Hữu cơ
- 2 câu Toán Hóa gồm 1 Vô cơ – 1 Hữu cơ
Mỗi câu mình trả lời 4 ý Đúng/Sai; Điểm số cho cũng mới lạ, như thế này:
- Đúng 1 ý trong 1 câu hỏi được 0,1 điểm
- Đúng 2 ý trong 1 câu hỏi được 0,25 điểm
- Đúng 3 ý trong 1 câu hỏi được 0,5 điểm
- Đúng 4 ý trong 1 câu hỏi được 1 điểm
Các câu có ghi năm màu đỏ và đáp án tô màu đỏ là lấy trong đề thi chính thức của Bộ GD năm đó; các câu còn lại là của giang hồ trên Internet!.
Câu dẫn Phần II trong đề thi lần đầu – năm 2025 như thế này nè:
Phần II. Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai.
Nội dung bài viết
Một nhà máy sản xuất sodium hydroxide (NaOH) và chlorine (Cl2) [2025]
bằng phương pháp điện phân dung dịch sodium chloride (NaCl) có màng ngăn với điện cực theo phương trình hóa học sau:

Sodium hydroxide rắn thu được bằng cách cô đặc rồi hạ nhiệt độ dung dịch chứa NaOH sau điện phân.
a) Trong quá trình điện phân, dung dịch ở khu vực cathode có pH < 7. S
Đơn giản mình nhìn vào ptr điện phân trên – thấy có tạo ra NaOH – là kiềm nên pH >7. Cao cấp hơn mình nói: bên cathode có OH – sinh ra – tạo trường kiềm nên trị pH > 7; phản ứng xảy ra ở mỗi điện cực là
- Cathode (cực âm): 2H2O + 2e → H2 + 2OH–
- Anode (cực dương): 2Cl– → Cl2 + 2e
b) Màng ngăn giúp ngăn phản ứng giữa sodium hydroxide và chlorine trong quá trình điện phân. Đ
Vì phản ứng giữa NaOH và Cl2 sẽ tạo nước Javel, khiến ta hổng thu được NaOH, khí Cl2
c) Tại anode, khí chlorine thu được do sự oxi hóa ion chloride. Đ
Hãy xem phương trình điện phân trên, trong đó ion Cl– là chất khử – ta nói nó bị oxi hóa!
d) Sodium hydroxide rắn thu được từ dung dịch chứa NaOH bằng phương pháp chiết. S
Vì NaOH rắn thu được bằng phương pháp kết tinh (câu nói trong đề: cô đặc rồi hạ nhiệt độ dung dịch chứa NaOH sau điện phân)
😘
Tơ capron là loại tơ có tính dai, [2025]
độ đàn hồi và độ bóng cao, ít thấm nước và được sử dụng để dệt vải may mặc. Tơ capron được tổng hợp từ caprolactam theo phương trình hóa học sau:
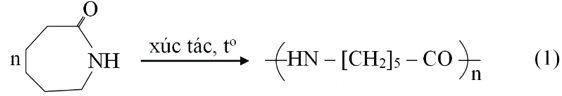
a) Trong phản ứng (1), các phân tử monomer bị mở vòng. Đ
Vì rõ ràng mình thấy vòng bị bể ra thành dây dài mà!
b) Tơ capron là tơ bán tổng hợp. S
Vì là tơ tổng hợp (100% do con người dùng hóa chất tổng hợp ra polime)
c) Do tơ capron và tơ nylon-6,6 đều có các nhóm –CO–NH– nên hai loại tơ này đều bền với dung dịch kiềm mạnh. S
Vì chúng bị thủy phân (bị chia tách) trong acid hoặc kiềm (tức không bền)
d) Do tơ capron có các nhóm –CO–NH– nên tơ capron là peptide. S
Vì muốn gọi là peptide, monome ban đầu phải là một α-aminoacid. Caprolactam hổng phải là α- ; nên nhóm –CO–NH– trong tơ capron được gọi tên là liên kết amide, và do vây, tơ capron được gọi là polyamide.
😍
Trong phòng thí nghiệm, một nhóm học sinh [2025]
tìm hiểu ảnh hưởng của thời gian lưu giữ tới nồng độ FeSO₄ trong dung dịch. Giả thuyết của nhóm học sinh là: “Khi để lâu, nồng độ FeSO4 trong dung dịch giảm.” Nhóm học sinh chuẩn bị 250,0 mL dung dịch FeSO4 (nồng độ khoảng 0,1 M) đựng trong bình kín (dán nhãn bình là Y) và tiến hành các thí nghiệm ở hai thời điểm khác nhau như sau:
-Ngày thứ nhất:
- Bước 1: Lấy 10,00 mL dung dịch trong bình Y cho vào bình tam giác rồi thêm tiếp 5 mL dung dịch H2SO4 2 M.
- Bước 2: Chuẩn độ dung dịch trong bình tam giác bằng dung dịch KMnO4 2,20×10⁻2 M đến khi xuất hiện màu hồng nhạt (bền trong khoảng 20 giây) thì dừng. Ghi lại thể tích dung dịch KMnO4 đã dùng.
- Lặp lại thí nghiệm chuẩn độ thêm 2 lần. Thể tích trung bình của dung dịch KMnO4 sau 3 lần chuẩn độ là 10,70 mL. Nồng độ của Fe(II) xác định được là C1 M.
-Ngày thứ tám:
Xác định lại hàm lượng Fe(II) của dung dịch chứa trong bình Y theo các bước tương tự như ngày thứ nhất. Thể tích trung bình của dung dịch KMnO4 sau 3 lần chuẩn độ là 9,92 mL. Nồng độ của Fe(II) xác định được là C2 M.
Nồng độ dung dịch KMnO4 như nhau trong các thí nghiệm chuẩn độ. Sự thay đổi nồng độ của Fe(II) (q%) được tính theo công thức: ![]()
a) Khi chuẩn độ, dung dịch KMnO₄ được nhỏ trực tiếp vào bình tam giác từ dụng cụ kí hiệu là (B) được minh họa ở Hình 1. S
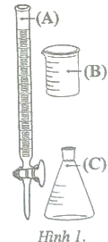 Vì phải cho vào (A) – gọi là buret để xác định điểm tương đương và đo được thể tích dung dịch KMnO4 chính xác ở thời điểm đó
Vì phải cho vào (A) – gọi là buret để xác định điểm tương đương và đo được thể tích dung dịch KMnO4 chính xác ở thời điểm đó
b) Giá trị của q là 7,9. (Kết quả các phép tính trung gian không được làm tròn, chỉ kết quả cuối cùng được làm tròn đến hàng phần mười) S
Vì q = 7,3. Xem bài giải bên dưới nha
c) Giá trị của C2 là 0,109. (Kết quả các phép tính trung gian không được làm tròn, chỉ kết quả cuối cùng được làm tròn đến hàng phần nghìn) Đ
Xem bài giải bên dưới nha
d) Kết quả thu được từ các thí nghiệm phù hợp với giả thuyết ban đầu của nhóm học sinh. Đ
Vì sau 8 ngày nồng độ FeSO4 giảm 7,3% – câu này biết chắc là Đúng luôn, vì mình nhớ dung dịch Fe2+ rất không bền, sẽ chuyển nhanh chóng thành Fe3+; hoặc thấy VddKMnO4 lần sau (9,92 mL) dùng để phản ứng với FeSO4 ít hơn lần đầu (10,70 mL) – tức lượng FeSO4 đã ít hơn rồi!
BÀI GIẢI
Phương trình chuẩn độ: 10FeSO4 + 2KMnO4 + 8H2SO4 → 5Fe2(SO4)3 + K2SO4 + 2MnSO4 + 8H2O
Phương trình cho nhận electron:
- Fe2+ → Fe3+ + 1e
- Mn7+ + 5e → Mn2+
Từ ptr chuẩn độ hoặc ptr cho nhận electron, bé thấy
molFeSO4 = 5molKMnO4 ⇔ CFeSO4.VFeSO4 = 5CKMnO4.VKMnO4
Lấy công thức trên tính cho ngày thứ 1 và ngày thứ 8. Cái mình tìm là CFeSO4 còn lại trong bình ở 2 ngày; mà ngày thứ 1 họ ghi là C1; ngày thứ 8 họ ghi là C2
Ngày thứ nhất, đề đã cho:
- VFeSO4 = 10,00 mL
- CKMnO4 = 2,20×10⁻2 M
- VKMnO4 = 10,70 mL
Vậy C1.10 = 5.2,20×10⁻2.10,7
⟹ tính ra C1 = 0,1177 M
Ngày thứ tám, đề đã cho:
- VFeSO4 = 10,00 mL
- CKMnO4 = 2,20×10⁻2 M
- VKMnO4 = 9,92 mL
Vậy C2.10 = 5.2,20×10⁻2.9,92
⟹ tính ra C2 = 0,10912 M
Tính tiếp sự thay đổi nồng độ
q = [(0,1177 – 0,10912).100%] : 0,1177 = 7,2897% ~ 7,3%
🤗
Trong phòng thí nghiệm, benzoic acid [2025]
được điều chế từ toluene theo sơ đồ gồm hai giai đoạn được đánh số (1) và (2) như sau:
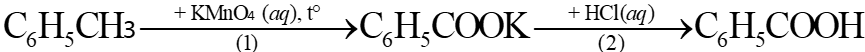
Trong một thí nghiệm tổng hợp benzoic acid theo sơ đồ trên, từ 2,0 mL toluene (khối lượng riêng bằng 0,867 g L⁻¹) thu được 1,40 gam benzoic acid. Biết KMnO4 và HCl được lấy dư. Hiệu suất của quá trình tổng hợp benzoic acid từ toluene là h%.
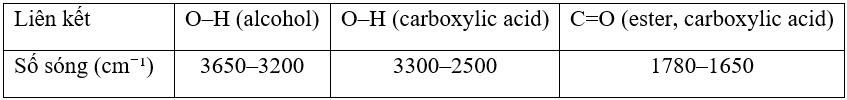
Cho biết số sóng hấp thụ đặc trưng của một số liên kết trên phổ hồng ngoại như sau:
a) Giá trị của h là 60,9. (Kết quả các phép tính trung gian không được làm tròn, chỉ kết quả cuối cùng được làm tròn đến hàng phần mười.) Đ
Xem bài giải bên dưới nha
b) Trong phản ứng với KMnO4 (aq) ở giai đoạn (1), toluene đóng vai trò là chất oxi hóa. S
Vì mình nhớ KMnO4 luôn luôn là chất oxi hóa (do Mn có số oxi hóa +7 cao nhất rồi); nên Toluene phải là chất khử!
c) Trên phổ hồng ngoại của benzoic acid, tín hiệu (peak) ở 1690 cm⁻¹ đặc trưng cho liên kết O–H. S
Vì benzoic acid có nhóm O-H (carboxylic acid) có tín hiệu đặc trưng ở 3300 – 2500 cm-1
d) Trong phản ứng ở giai đoạn (2), anion C6H5COO⁻ là một base theo thuyết Brønsted – Lowry. Đ
Vì ion C6H5COO– (trong C6H5COOK) nhận proton (H+của HCl):
C6H5COO– + H+ → C6H5COOH
BÀI GIẢI
mtoluene = V.D = 2.0,867 = 1,734 g
Từ sơ đồ phản ứng C6H5-CH3 (92 g) → C6H5-COOH (122 g)
Vậy với 1,734 g Toluene ta sẽ thu được 2,299434783 g Benzoic acid (gọi là lượng tính theo lí thuyết, tức giả vờ hiệu suất 100% – lượng Toluene chuyển hoàn toàn thành Acid, không bị rơi rớt miếng nào hết!).
Nhưng đề nói chỉ thu được 1,40 gam Acid thôi.
Nên hiệu suất là h = (1,4 : 2,299434783).100% ~ 60,9%
😘
Liên kết nhanh
Đọc thêm các bài viết về thi tốt nghiệp THPT tại đây nhe!
Viết bởi Đỗ Trọng Toan từ W3chem.com
Mình là người tự thực hiện toàn bộ dự án này – bao gồm xây dựng trang web, viết nội dung, tìm tài liệu tham khảo, trả lời câu hỏi bạn gởi về. Vui lòng xem xét QUYÊN GÓP để hỗ trợ W3chem CHỈ BẰNG CÁCH CHIA SẺ BÀI VIẾT NÀY LÊN MẠNG XÃ HỘI; bởi vì trong tương lai, bạn sẽ cho mình nhiều thời gian để làm việc trên W3chem, cũng có nghĩa bạn nhận thêm nhiều nội dung mới nhanh hơn tại đây.😍 🥰 😘





