Kim loại có tính chất vật lí và tính chất hoá học thế nào?
Kim loại có nhiều tính chất vật lý qúy giá, sử dụng rất nhiều trong cuộc sống hiện đại. Rất khó để tưởng tượng …thế giới sẽ ra sao nếu không có kim loại.

Kim loại vàng (Au) do có tính chất hóa học (tính khử) quá yếu; nên tồn tại trường tồn-không biến đổi theo thời gian …và vì vậy …chúng trở nên vô giá. Mấy ngày nay của tháng 11-2021, giá 1 lượng vàng trong nước đã vượt 60 triệu VNĐ; vì vậy mà nhiều người tiếc rẻ: vàng lên cao quá, mua vô thì không đủ tiền; bán ra thì không có vàng để bán …thật khổ tâm quá đi thôi! …hê …hê …hê
Nội dung bài viết
1. Nguyên tố kim loại ở đâu trong bảng tuần hoàn?
1.1. Nhiều nguyên tố kim loại lắm
Kim loại xuất hiện trong bảng tuần hoàn từ nhóm IB đến tận VIIIB; từ nhóm IA đến VIA (trong đó, có nhóm A chứa hoàn toàn là kim loại, có nhóm A chỉ 1 phần là kim loại).
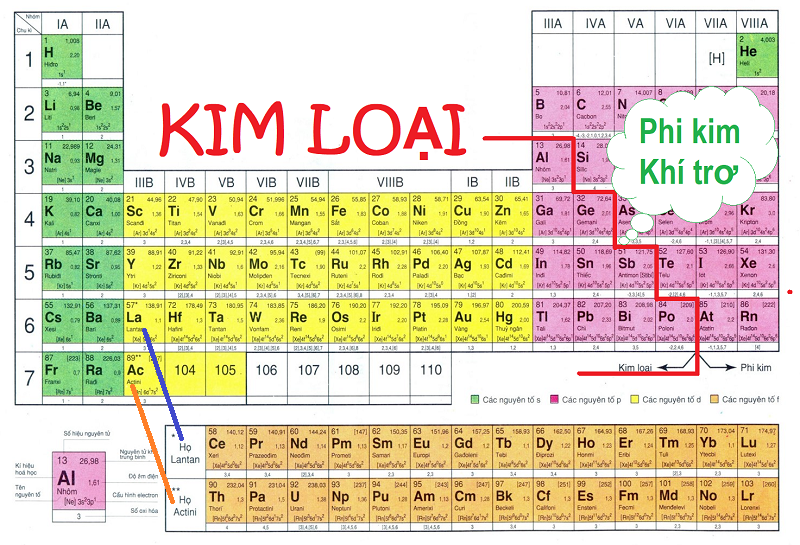
Kim loại chuyển tiếp: nhóm tô màu vàng và màu nâu; tức các kim loại nhóm IB đến VIIIB.
1.2. Đặc điểm nguyên tử kim loại
+Đa số_hầu hết (không phải tất cả) kim loại có 1, 2 hoặc 3 electron ở lớp ngoài cùng (do có ngoại lệ, xem bảng tuần hoàn là thấy ngay).
+Những nhận xét sau dựa trên bài Sự biến đổi tính chất theo chu kì và theo nhóm A; một bài học dễ thương ở lớp 10.
Những nguyên tố trong nhóm kim loại IA, IIA, IIIA được sắp xếp từ trên xuống dưới theo chiều
- điện tích hạt nhân nguyên tử (số thứ tự, số Z) tăng dần.
- năng lượng ion hoá giảm dần (tức tính kim loại, tính khử tăng dần).
- bán kính nguyên tử tăng dần (do số Z, tức số electron tăng làm số lớp electron tăng luôn).
Trong một chu kì, từ trái qua phải, tính kim loại giảm dần (giống dãy điện hoá!). So với nguyên tử PHI KIM cùng chu kì, nguyên tử KIM LOẠI:
- có Rnguyên tử lớn hơn.
- có (năng lượng ion hoá) I nhỏ hơn.
- có số electron ở các phân lớp ngoài cùng ít hơn.
- dễ nhường electron trong các phản ứng hoá học.
2. Đơn chất kim loại cấu tạo thế nào?
Đơn chất kim loại tồn tại ở dạng mạng tinh thể.
Mạng tinh thể kim loại gồm có nguyên tử – ion kim loại – các electron (chuyển động) tự do. Mạng tinh thể của kim loại trong chương trình (hiện nay đang giảm tải!) gồm:
LẬP PHƯƠNG TÂM KHỐI gồm
- tất cả kim loại IA (Li Na K Rn Cs)
- chỉ kim loại Ba ở IIA
- Cr
- Feα
LỤC PHƯƠNG gồm: Be và Mg ở nhóm IIA
LẬP PHƯƠNG TÂM DIỆN gồm
- Ca và Sr ở nhóm IIA
- Al
- Feγ
Mạng tinh thể ảnh hưởng đến tính chất vật lý:
- các tính chất vật lí nhiệt độ nóng chảy, nhiệt độ sôi và khối lượng riêng của các kim loại kiềm IA biến đổi có qui luật.
- ở kim loại kiềm thổ IIA lại biến đổi không theo một quy luật nhất định (do các kim loại kiềm thổ IIA có kiểu mạng tinh thể hổng giống nhau).
3. Tính chất vật lí chung của kim loại
Những tính chất vật lí chung của kim loại là tính dẻo, dẫn điện, dẫn nhiệt, có ánh kim_vẻ sáng kim loại ; gây nên chủ yếu bởi các electron (chuyển động) tự do trong tinh thể kim loại.
- Các kim loại khác nhau có độ dẫn điện, dẫn nhiệt khác nhau do có mật độ electron tự do khác nhau.
- Độ dẫn điện, độ dẫn nhiệt của Ag>Cu>Au>Al>Fe (bạc đồng ăn nhôm sắt!)
Ứng dụng:
…
4. Tính chất vật lí riêng của kim loại
Các tính chất sau của kim loại phụ thuộc vào độ bền của mạng tinh thể, khối lượng riêng, kiểu mạng tinh thể của kim loại.
| Li (Liti) Os (Osimi) | nhẹ nhất (có khối lượng riêng nhỏ nhất) nặng nhất (có khối lượng riêng lớn nhất) |
| Hg (thuỷ ngân) W (Vonfam) Cs (xesi) | tnc thấp nhất tnc cao nhất tnc thấp nhất trong các kim loại kiềm (Na, K, Rb, Cs) |
| Cr (crom) Cs (xesi) | cứng nhất mềm nhất |
| Au (vàng) | dẻo nhất |
Lưu ý: Thủy ngân (Hg) là kim loại thể lỏng (duy nhất) ở t0 phòng. Hơi Hg rất độc, gây chết người hoặc rất nhiều bệnh nan y. Vì vậy mà ông vua Tần Thủy Hoàng đã trữ một khối lượng Hg khổng lồ xung quanh hầm mộ của mình; để hậu thế khỏi đào bới. Bạn cũng nên biết cách xử lý Thủy ngân nếu chẳng may nhiệt kết Thủy ngân (thiết bị y tế rất thông dụng) rơi vỡ.
5. Tính chất hóa học chung của kim loại
Bạn cần nhớ về kỉ niệm đẹp của 2 năm trước đây: Phản ứng oxi hóa khử là gì?
Tính chất hoá học chung của kim loại: tính khử-tính cho (nhường) electron. Nói cách khác, kim loại dễ bị oxi hoá thành ion dương:
M – ne → Mn+ (viết là M → Mn+ + ne)
5.1. Phản ứng với H2O
5.1.1. Kim loại mạnh: nhóm IA, IIA và Nhôm (Al)
- Ở t0 thường, tất cả IA (Li Na K Rb Cs) và ba kim loại cuối IIA (Ca Sr Ba) tan được trong nước ở t0 thường tạo dung dịch kiềm mạnh. Ví dụ:
2Na + 2H2O → 2NaOH + H2
Ca + 2H2O → Ca(OH)2 + H2
Nhớ thêm oxit tương ứng của các kim loại trên như Li2O Na2O …CaO SrO BaO cũng vây; nhưng hay viết sai phản ứng. Nhớ là
Na2O + H2O → 2NaOH
CaO + H2O → Ca(OH)2
- Al và 2 kim loại còn lại ở IIA (Be Mg)
Be không tác dụng, ngay cả ở t0 cao.
Mg, ở t0 thường tác dụng chậm tạo Mg(OH)2; ở t0 cao tác dụng nhanh với hơi nước
Mg + 2H2O → Mg(OH)2 ít tan + H2
Mg + H2O hơi → MgO + H2
Al tác dụng được với H2O nhưng phản ứng dừng lại lập tức do tạo tủa Al(OH)3 bao bọc lá Al.
2Al + 6H2O → 2Al(OH)3 kết tủa + 3H2
5.1.2. Kim loại trung bình: Mn Zn Cr Fe Co Ni Sn Pb tác dụng với H2O ở t0 cao
3Fe + 4H2O —t0< 570 0C–→ Fe3O4 + 4H2
Fe + H2O —t0> 570 0C–→ FeO + H2
5.1.3. Kim loại yếu: Cu Hg Ag Pt Au
Không tác dụng với nước dù ở t0 cao!
5.2. Nhúng kim loại trong dung dịch muối
5.1.2. Lưu ý các kim loại tác dụng với nước ở t0 thường tạo dung dịch kiềm:
không “đẩy” được kim loại sau ra khỏi dung dịch muối, do chúng bận tác dụng với H2O rồi.
- Ví dụ cho kim loại Na vào dung dịch MgSO4
Đừng viết SAI là 2Na + MgSO4 → Na2SO4 + Mg
Mà lúc đầu có sủi bọt khí mạnh do Na + H2O → NaOH + 1/2H2
sau đó có kết tủa keo màu trắng do 2NaOH + MgSO4 → Mg(OH)2 tủa + Na2SO4
- Ví dụ cho kim loại Na vào dung dịch CuSO4
Đừng viết SAI là 2Na + CuSO4 → Na2SO4 + Cu
Mà lúc đầu có sủi bọt khí mạnh do Na + H2O → NaOH + 1/2H2
sau đó có kết tủa màu xanh lam do 2NaOH + CuSO4 → Cu(OH)2 tủa + Na2SO4
- Ví dụ cho từ từ kim loại Na đến dư (!) vào dung dịch AlCl3
Đừng viết SAI là 3Na + AlCl3 → 3NaCl + Al
Mà lúc đầu có sủi bọt khí mạnh do Na + H2O → NaOH + 1/2H2
sau đó có kết tủa keo trong-trắng do 3NaOH + AlCl3 → Al(OH)3 tủa + 3NaCl
rồi kết tủa tan dần đến hết tạo dung dịch không màu do Al(OH)3 + NaOH → NaAlO2tan + 2H2O
- Ví dụ cho từ từ kim loại Ba đến dư (!) vào dung dịch Al2(SO4)3
Đừng viết SAI là 3Ba + Al2(SO4)3 → 3BaSO4 + 2Al
Mà lúc đầu có sủi bọt khí mạnh do Ba + 2H2O → Ba(OH)2 + H2 ; tạo dung dịch có Ba2+, OH–
tiếp theo sẽ xuất hiện kết tủa màu trắng; rồi kết tủa tan một phần mà không tan hết do:
Ba2+ + SO42- → tủa BaSO4 không tan
Al3+ + 3OH– → tủa Al(OH)3 nhưng tan hết trong OH– dư
5.2.2. Các kim loại không tác dụng với nước ở t0 thường;
ta sử dụng câu nói quen thuộc ở lớp 8 , 9 là: kim loại đứng trước “đẩy” kim loại đứng sau ra khỏi dung dịch muối. Ví dụ nhúng cây đinh sắt (Fe) vào dung dịch CuSO4 thì
Fe + CuSO4 dung dịch xanh lam → FeSO4 dung dịch xanh lục rất nhạt + Cu
Hiện tượng:
- đinh Fe tan ra (bị bào mòn ở phần nhúng trong dung dịch); đồng thời xuất hiện lớp kim loại màu đỏ (Cu) bám vào.
- dung dịch CuSO4 ban đầu màu xanh lam dần bị nhạt bớt màu …do dung dịch sau phản ứng là FeSO4.
5.3. Phản ứng với axit
5.3.1. Kim loại phản ứng với axit HCl, H2SO4 loãng

Viết vài phản ứng của kim loại với trường hợp hai axit này
| 2Na + 2HCl → 2NaCl + H2 | Na + H2SO4 loãng → Na2SO4 + H2 |
| Mg + 2HCl → MgCl2 + H2 | Mg + H2SO4 loãng → MgSO4 + H2 |
| Fe + 2HCl → FeCl2 + H2 | Fe + H2SO4 loãng → FeSO4 + H2 |
| 2Al + 6HCl → 2AlCl3+ 3H2 | 2Al + 3H2SO4 loãng → Al2(SO4)3 + 3H2 |
| Cu + HCl –x-→ | Cu + H2SO4 loãng –x-→ |
| Ag + HCl –x-→ | Ag + H2SO4 loãng –x-→ |
Các phản ứng trên cân bằng quá dễ, chỉ cần biết đếm, biết chữ và biết viết là mình làm được! Nhưng …những phản ứng tiếp theo đòi hỏi bạn học nghiêm túc Hóa lớp 10:
- Phải hiểu và biết cách tính số oxi hóa.
- Nếu đã trót dại học chểnh mảng phần cân bằng …thì vui vẻ xem lại tại đây, Hướng dẫn chi tiết 5 bước cân bằng phản ứng oxi hóa khử.
5.3.2. Kim loại phản ứng với axit HNO3, H2SO4 đặc


5.3.3. Lưu ý
- Fe + axit HNO3 dư , axit H2SO4đặc dư → Fe3+ (lớp10, 11).
- Fe dư + axit HNO3 , axit H2SO4đặc → Fe3+ —+Fe dư–→ Fe2+ (lớp 12).
- Al, Cr, Fe không tác dụng được với dung dịch HNO3 đặc nguội ; dung dịch axit H2SO4 đặc nguội. Nếu đặc nóng thì Al, Cr, Fe mới phản ứng.
- Au, Pt chỉ phản ứng được với nước cường toan (nước cường thuỷ, là hỗn hợp của 1VHNO3 và 3VHCl dung dịch đặc):
Au + 1HNO3 + 3HCl → AuCl3 + NO + 2H2O
5.3.4. Nói chung
- với Fe và kim loại sau Fe thì H2SO4 đặc → SO2 ; HNO3 loãng → NO.
- với kim loại trước Fe, tạo mọi sản phẩm khử của N+5, S+6.
- HNO3 đặc luôn tạo NO2 với mọi kim loại.
- kim loại có tính khử mạnh như Mg, Al, (có khi đề cho Zn) ⇒ thường tạo muối NH4NO3 (cảnh giác khi đề không có câu “sản phẩm khử duy nhất” hay “không còn sản phẩm khử nào khác”).
- đề hổng nói gì hết thì
- HNO3loãng → NO
- HNO3đặc →NO2
- H2SO4đặc → SO2
5.3.5. Mở rộng
H2SO4 đặc có tính hút nước rất mạnh nên dùng làm khô các chất khí (các chất khí này phải không tác dụng được với H2SO4 đặc như khí Cl2, N2, O2, NO, NO2, CO2, . . . )
H2SO4 đặc, HNO3 loãng-đặc tác dụng được với phi kim (C, P, S) và một số chất khử khác.
Liên kết nhanh
Đọc thêm các bài viết về Kim loại và Hóa lớp 12 tại đây.
Đừng quên chia sẻ bài viết lên mạng xã hội để nhiều người cùng học nha bạn.







