Hướng dẫn thêm về orbital nguyên tử (AO)
Hai người đàn ông đang chuẩn bị những quả bóng hình cầu để bán. Khi tôi nói họ đang bán Orbital s; một người ngạc nhiên và nhìn tôi với gương mặt dè chừng! Có lẽ họ nghĩ tôi khùng!

Con người và mọi vật chất đang sống-tồn tại trong hệ trục tọa độ 3 chiều (chiều dài, rộng, cao) Ox, Oy, Oz. Nguyên tử, phân tử, các AO cũng không ngoại lệ.
Orbital nguyên tử, nói đơn giản là ngôi nhà có hình dáng xác định; trong ngôi nhà đó, các electron (nhiều nhất là 2 e) chuyển động hỗn loạn với tốc độ tia chớp-nhanh đến nỗi xuất hiện liên tục tại mọi vị trí trong AO, tạo nên hình ảnh như “đám mây”; bôi dày đặc toàn bộ AO.
Nguyên tắc để electron di chuyển trong 1 AO phù hợp là mức năng lượng nó mang trong người. Cũng giống như bạn, nếu bạn chỉ di chuyển trong vùng không gian là các nhà hàng sang trọng, thì số tiền bạn có rất khủng!
Trong lúc đó, hạt nhân nguyên tử (các hạt p và n) yên vị tại tâm hệ trục tọa độ Oxyz như hình dưới đây:
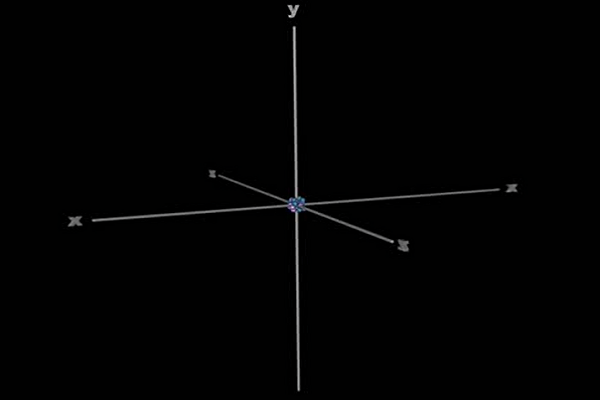
Electron chuyển động trong 4 loại AO cơ bản sau
1 orbital s (1 ngôi nhà hình s)
AO loại s là 1 khoảng không gian có hình cầu (nhớ phân biệt hình tròn với hình cầu nha bạn). Vì chỉ là 1 khoảng không gian nên AO-s chỉ chứa tối đa 2 electron; hóa học kí hiệu là s2.

3 orbital p (3 ngôi nhà hình p)
AO loại p là 3 khoảng không gian có hình số 8 nổi, mỗi AO nằm dọc 1 trục tọa độ Ox, Oy, Oz (bạn có thể tưởng tượng bằng cách lấy 2 quả bóng hình quả lê cột vào nhau; hoặc món thịt xiên que nướng). Vì có đến 3 khoảng không gian nên AO-p chỉ chứa tối đa 6 electron; hóa học kí hiệu là p6.

5 orbital d (5 ngôi nhà hình d)
AO loại d là 5 khoảng không gian có hình rất xinh đẹp (bạn xem hình và tưởng tượng). Vì có đến 5 khoảng không gian nên AO-d chứa tối đa 10 electron; hóa học kí hiệu là d10.


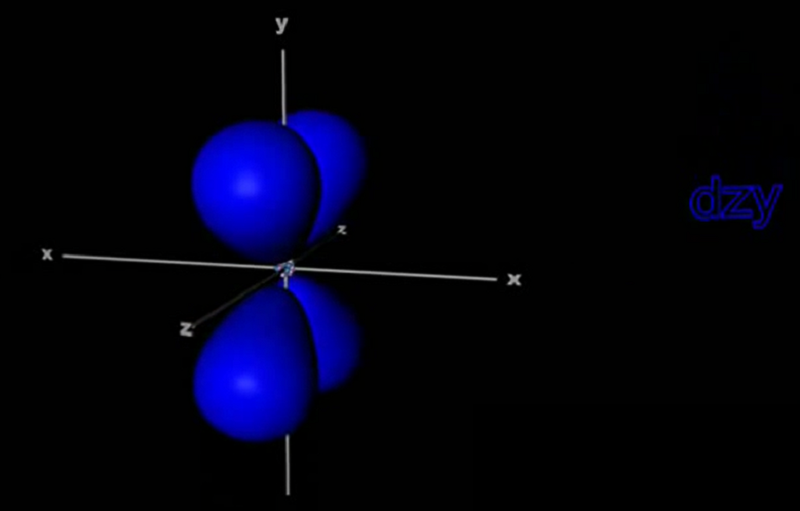


7 orbital f (7 ngôi nhà hình f)
Các AO-f quá phức tạp; có 7 AO-f với 7 thể hình khác nhau. Vì có đến 7 khoảng không gian nên AO-f chứa tối đa 14 electron; hóa học kí hiệu là d14.
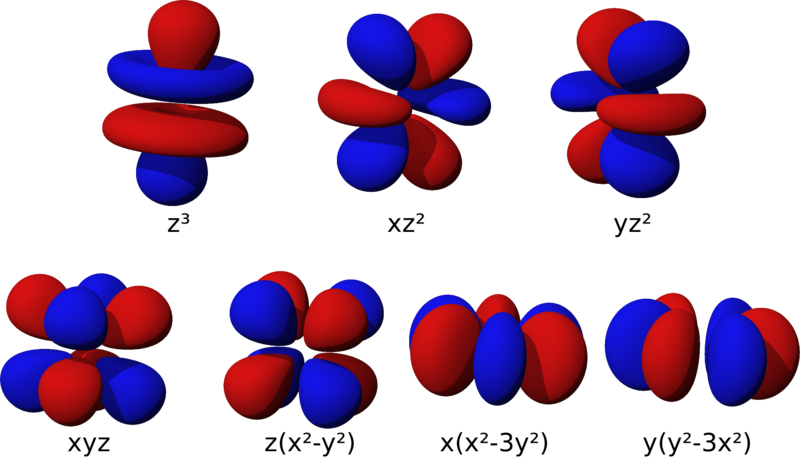
Hình dạng của nguyên tử khi vẽ AO
Nếu gộp các khoảng không gian (các AO) s, p, d trên vào 1 hình, thì hình dạng lớp vỏ nguyên tử lúc này quá khủng khiếp. Trong hình dưới đây, 1 AO-s và 3 AO-p nằm ở bên trong bị che khuất không thấy, hầu như bạn chỉ thấy các 5 AO-d bên ngoài thôi!

Vẽ nguyên tử thế nào cho tuổi teen dễ hiểu?
Ở bài vỡ lòng về nguyên tử, bạn có nhớ hình ảnh trái bắp Mỹ có ruột vàng ươm và nhiều lớp vỏ mảnh mai bên ngoài không? Hình ảnh nguyên tử bạn đã gặp hao hao giống vậy, bởi vì qúa dễ hiểu. Như hình dưới đây, loại nguyên tử Neon có hạt nhân chứa 10p, 10n; vỏ có 2 lớp: lớp trong chứa 2e, lớp ngoài chứa 8e.
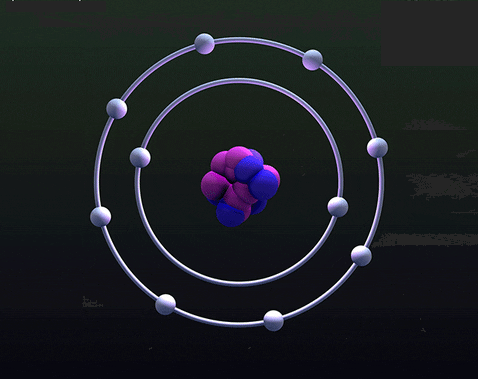
Giờ đây bạn sẽ hiểu, lớp vỏ nguyên tử không phải giống như lớp vỏ trái bắp-tức từng lớp có ịn electron và nằm chồng chập nhau như hình nguyên tử Argon trên.
Trong nguyên tử, các electron di chuyển “búa xua” len lỏi từ vùng ngoài cho đến vùng sát hạt nhân nguyên tử; nhưng giới hạn trong vùng không gian hình dạng xác định (gọi là AO); vậy trong nguyên tử, sẽ có 1AO (như nguyên tử H, He) hoặc có rất nhiều AO chồng chập lên nhau. Như nguyên tử Argon trên, nếu vẽ AO gần đúng bản chất, bạn sẽ có hình sau đây:
- 2e chạy trong 1AO-s hình cầu nhỏ phía trong cùng.
- 2e chạy trong 1AO-s hình cầu lớn hơn như hình.
- 6e chạy trong 3 AO-p hình số tám nổi.
- sau này thay vì nói như trên, bạn sẽ viết dãy gọn gàng như sau: 1s2 2s2 2p6.
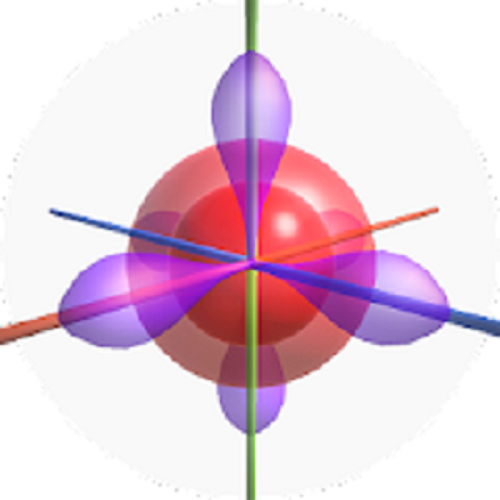
Nếu bạn nhìn nguyên tử vẽ kiểu này, chắc có thể ai đó bị hoa mắt chóng mặt;
cho nên…
cách vẽ lớp vỏ electron như vỏ trái bắp (từng lớp đính hạt electron) nhìn thân thiện với tuổi teen hơn!
Đừng quên chia sẻ bài viết lên mạng xã hội để nhiều người cùng học nha bạn.







Bài rất hay và dễ hiểu, hình minh họa cụ thể
Cám ơn Nguyen. Rất mong gặp lại bạn ở các bài viết khác.
Giờ đây già U50, do kèm con nhỏ học “Hoa Hậu” “Hoá Học”, mới đi tìm hiểu lại nàng “hoa hậu” ngày xưa đã từng yêu từng ghé để tìm cách truyền đạt ngắn gọn, xúc tích, gần gủi và đặc biệt DỂ HIỂU đối với trí tuệ của cháu thì nhận thấy THẦY giảng làm cho tôi “yêu say đắm nàng hoa hậu hoá học đỏng đảnh kiêu sa” ngày còn cắp sách đến Trường! Chúc Thầy luôn mạnh khoẻ!
Chào anh QUYPV,
Đọc bài viết thấy Anh rất tiếu lâm duyên dáng, điều này áp dụng khi học môn Hóa thì tuyệt vời.
Đúng là học môn Hóa ở VN mình là đau khổ lắm; do mọi người tưởng tượng viễn vông – mơ mộng, ngồi suy diễn và chế ra vô số câu hỏi trên trời, làm con cái chúng ta mệt mỏi lắm. Chúc Anh tìm được cách dạy môn Hóa cho cháu một cách tự nhiên & dễ hiểu.
Rất cám ơn Anh QUYPV vì đã “quằn quại” do mất ngủ nhiều đêm, có lẽ vài bài viết đã vô tình khiến Anh day dứt với thuở yêu ban đầu say đắm ấy!.
Có câu hỏi gì từ cháu mời Anh viết lên đây, tôi sẽ cố gắng trong khả năng để giải đáp.
Chúc Anh và Gia đình nhiều sức khỏe, hạnh phúc và thành đạt.
Trân trọng,
Toan từ W3chem.com.