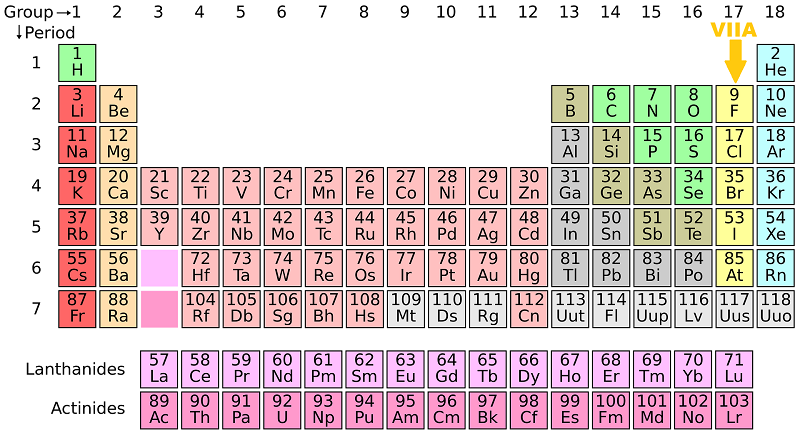
Halogen (F, Cl, Br, I ở nhóm VIIA) có gì đặc biệt ?
Một lời tỏ bày trên Facebook: Con người có thể “tha hóa”. Nhưng hóa sẽ không bao giờ tha con người!
Bạn mến, Hóa quý trọng và không bỏ rơi ai!; bạn có thể tàn nhẫn xé tập Hóa, ngó lơ Giáo viên, … nhưng Hóa vẫn da diết, sẽ không ruồng bỏ.
Halogen là bài học nhẹ nhàng nhưng sâu lắng, giúp bạn trải nghiệm một chặng đường đời có hoa, có cỏ và có cả Hóa !!!. Tục ngữ có câu”Kiến tha lâu đầy tổ”; W3chem kỳ vọng, bạn sẽ “tha Hóa”, cần cù và nhẫn nại – mỗi ngày như kiến ngoan; đương nhiên bạn đã giỏi!

Nội dung bài viết
1. Vì sao là Halogen mà không phải là Halloween?
Halogen, từ gốc tiếng Hy Lạp: hal – muối và gen – tạo ra; bởi vì chúng đều phản ứng với kim loại kiềm (IA), kim loại kiềm thổ (IIA) tạo muối dạng tinh thể ion ổn định, trong đó hai muối rất phổ biến – đến nỗi ngày nào chúng mình cũng phải dùng là natri clorua NaCl (muối ăn được) và canxi florua CaF2 (là thành phần kem đánh răng).
2. Halogen là ai trong nhóm VIIA?
Nhóm VIIA trong bảng tuần hoàn gồm các nguyên tố: fluorine (F), chlorine (Cl), bromine (Br), iodine (I), astatine (At), Uus (một số bảng ghi tên là tennessine – Ts).
Trong các nguyên tố đó, At và Uus là 2 nguyên tố có tính phóng xạ (Uus còn là nguyên tố mới toanh hà); cả hai
- đều rất hiếm hoi.
- có thời gian sống ngắn (như 1 đồng vị bền của At chỉ sống được có 8 giờ) đến nỗi mà …nhiều tính chất chưa biết do chưa kịp nghiên cứu luôn!
- ⇒ nên Hóa học không thể nói gì nhiều về hai nguyên tố này; tốt nhất nên chuyển qua cho các nhà Vật lý hạt nhân nghiên cứu để học có việc làm.
Như vậy, nhóm halogen chỉ gồm các nguyên tố
F , Cl , Br , I
3. Cấu hình electron nguyên tử và vài điểm của halogen

4. Đơn chất của halogen
4.1. Tổng quát
Ở nhiệt độ phòng, VIIA là nhóm duy nhất có đơn chất
- đều ở dạng phân tử hai nguyên tử – kí hiệu chung là X2.
- tồn tại ở cả 3 trạng thái vật chất là khí – lỏng – rắn, trong đó
- F2 là chất khí màu lục nhạt
- Cl2 là chất khí màu vàng lục nhạt
- Br2 là chất lỏng màu nâu đỏ
- I2 là chất rắn màu tím đen đậm.

Các đơn chất F2, Cl2, Br2 có độc tính cao. Ngưỡng gây chết người của Cl2 là 98,6mg trong 1m3 không khí. Cl2 là vũ khí hóa học đầu tiên con người sử dụng trong chiến trang thế giới thứ nhất (từ tháng 8-1914 đến tháng 11-1918).
4.2. Question
520 gas cylinders containing 300,000 pounds of chlorine gas was used as a chemical weapon at Ypres, France in 1915. 5,000 soldiers died and 15,000 injured.
a) Air weighs 28.8 grams per mole. How many grams per mole does chlorine gas (Cl2) weigh?
b) Will chlorine gas stay close to the ground or rise up into the air?
c) How many grams is 300,000 lbs mentioned above, knowing that 1 lb = 454 grams.
d) How many moles of Cl2 is 300,000 lbs of Cl2?
520 chai khí chứa 300.000 pound khí clo được sử dụng làm vũ khí hóa học tại Ypres, Pháp vào năm 1915. Đã có 5.000 binh sĩ chết và 15.000 người bị thương.
a) Biết M trung bình của không khí là 28,8 gam/mol. Tính M của khí clo, Cl2?
b) Khí Cl2 sẽ ở gần mặt đất hay bay lên cao? Vì sao?
c) Có bao nhiêu gram khí Cl2 trong 300.000 pound trên? Biết 1 pound = 454 gam.
d) Có bao nhiêu mol khí Cl2 trong 300.000 pound trên?
5. Số oxi hóa của halogen
- Trong đơn chất, số oxi hóa của halogen đương nhiên bằng 0.
- Trong hợp chất, số oxi hóa của halogen được liệt kê dưới đây:
- F chỉ có duy nhất số oxi hóa -1
- Cl , Br , I ngoài số oxi hóa -1 còn có thêm +1 +3 +5 +7
Halogen là những phi kim mạnh nhất (tính phi kim là tính oxi hóa – tính nhận electron). Các nguyên tử halogen nhận 1 electron rất mãnh liệt.


Hai hình trên đều vẽ quá trình nhận 1 electron của F và Cl ; tuy nhiên sự thú vị hổng phải ở đây! Bạn hãy nhìn biểu cảm ở gương mặt của F, Cl; so sánh và đưa ra lời giải thích?
Để giải trí, mời bạn vui đọc nguyên tử chơi trò chơi kéo co !!!
6. Halogen có tính oxi hóa là chủ đạo (tính khử yếu thôi!)
Từ giá trị độ âm điện (F lớn nhất), số oxi hóa và thực nghiệm thấy:
- F chỉ có tính oxi hóa; và tính oxi hóa của F là vô địch!
F0 + 1e → F–
- Cl, Br, I có tính oxi hóa và cả tính khử; tuy nhiên tính oxi hóa là đặc trưng. Ví dụ mình sẽ thấy với Cl,
- tính oxi hóa: Cl0 + 1e → Cl–
- tính khử: Cl0 → [Cl+1 + 1e] [Cl+3 + 3e] [Cl+5 + 5e] [Cl+7 + 7e]
- và đương nhiên, tính oxi hóa của F > Cl > Br > I.
7. Phản ứng chứng tỏ tính oxi hóa của F>Cl>Br>I
7.1. Halogen gặp hydrogen
Các đơn chất halogen đều phản ứng với hydrogen (H2) tạo hydrogen halide (HX); nhưng điều kiện và cường độ phản ứng thể hiện khác nhau.
H2 + F2 → 2HF xảy ra ngay trong bóng tối, ở t0 thấp. Phản ứng mãnh liệt, phát ra tiếng nổ.
H2 + Cl2 → 2HCl xảy ra khi đun nóng hoặc ở 0 thường có chiếu tia tử ngoại. Phản ứng mạnh, phát ra tiếng nổ.
H2 + Br2 → 2HBr xảy ra khi đun nóng. Phản ứng chậm chạp.
H2 + I2 ⇌ 2HI chỉ xảy khi đun nóng. Phản ứng chậm và hai chiều (hiệu suất không đạt 100%), thu hỗn hợp gồm HI và H2 dư, I2 dư.
7.2. Halogen gặp nước
Khi cho các halogen vào H2O thì
- F2 có tính oxi hóa vô địch nên “đốt cháy” luôn nước, chỉ có tính oxi hóa.
- Cl2 và Br2 phản ứng thuận nghịch, thể hiện tính oxi hóa và tính khử.
- Còn I2 hầu như không phản ứng.
Phản ứng cụ thể như sau (bạn nhớ ghi thêm số oxi hóa vào mỗi phản ứng):
- 2F2 (aq) + 2H2O (l) → O2 (g) + 4HF (aq)
- Cl2 (aq) + H2O (l) ⇌ HCl (aq) + HClO (aq)
- Br2 (aq) + H2O (l) ⇌ HBr (aq) + HBrO (aq)
- I2 (s) + H2O (l) —x→
Ghi chú: theo SGK mới-áp dụng cho lớp 10 vào năm học 2022-2023, phương trình phản ứng sẽ ghi thêm trạng thái (viết tắt từ tiếng Anh) của mỗi chất. Cách viết này theo SGK nước ngoài, cụ thể
- s (solid): rắn
- g (gaz): khí / hơi
- l (liquid): lỏng
- aq (aqua): dung dịch
8. Liên kết nhanh
Halogen phản ứng hóa học với bạn bè như thế nào.
Đọc thêm các bài viết khác về Hóa lớp 10 tại đây.
Chia sẻ bài viết lên mạng xã hội







*Mặc dù khí Clo đã bị cấm sử dụng trong chiến tranh theo công ước La Haye năm 1907; nhưng chúng không chỉ được dùng làm vũ khí vào năm 1915 xa lắc xa lơ; mà còn được dùng ngay cả trong thế giới hiện nay. Em hãy nêu một vài hậu quả ghê gớm của vũ khí hóa học này?
*Giải thích vì sao F chỉ có soh là -1; trong khi Cl Br I còn có thêm soh +1 +3 +5 +7?
-Hậu quả của clo
+Hợp chất của clo được xếp vào nhóm các chất gây ung thư nhóm B đồng thời có khả năng gây dị tật đối với trẻ sơ sinh, gia tăng nguy cơ mắc phải bệnh tim mạch, hô hấp…
+Khi phản ứng với nước trong phổi, khí clo tạo ra axit hydrochloric và khiến nạn nhân chết nhanh chóng. Ở hàm lượng thấp, khí clo gây ho, nôn mửa và bỏng mắt.
F là phi kim mạnh nhất nên nó chỉ nhận thêm e => soh âm
* Khí clo có màu vàng xanh và có mùi tương tự thuốc tẩy. Nó là một tác nhân gây nghẹt thở, cản trở hô hấp và làm tổn hại các mô trong cơ thể. Clo có thể phản ứng với nước trong niêm mạc của phổi để tạo thành axit clohydric- chất kích thích có thể làm chết người.
* Vì F là phi kim mạnh nhất trong tất cả các phi kim nên trong phản ứng nó chỉ nhận thêm e nên luôn có số oxi hóa âm
– Clo gây hậu quả lên tóc:
Clo tách dầu ra khỏi tóc, làm cho các biểu bì tóc thiếu sự kết dính, lớp vỏ ngoài không được bảo vệ nên dễ dàng đứt gãy. Khi đó, tóc sẽ mất đi độ bóng mượt nên khó tạo hình, nếu nhuộm tóc thì màu nhuộm sẽ nhanh bị bay màu hơn.
– Vì Flo là phi kim mạnh nhất trong số tất cả các phi kim nên trong các phản ứng nó chỉ thu thêm 1e nên luôn luôn có số oxi hoá -1. Các halogen khác còn có số oxi hoá dương vì còn có những phi kim mạnh hơn chúng nên chúng có thể nhường e cho phi kim này.
Khí Clo kích thích hệ hô háp đặc biệt ở trẻ em và người cao tuổi. Trong trạng thái khí, clo kích thích các màng nhầy và khi ở dạng lỏng nó có thể làm cháy da. Khí Clo được xem là một hoá chất dạng khí cực độc có thể ggy tử vong và nhiều biến chứng nguy hiểm. Nếu như nhiễm Clo với nồng độ cao quá mức cho phép có thể tạo ra sự phồng rộp phổi, tích tụ huyết thanh trong phổi. Với mức độ phơi nhiễm nồng độ thấp, kéo dài lâu năm có thể làm phổi suy yếu, rối loạn hô hấp.
Do nguyên tử F có phân lớp ngoài cùng là 2p. Phân lớp này không ở gần phân lớp d nào nên không thể kích thích các e hoá trị ghép đôi sang các obitan d để đạt trạng thái kích thích chứa nhiều e độc thân hơn, do đó chỉ có soh -1.
1. Thông thường, hàm lượng Clo tồn tại trong nước nếu ở mức cho phép theo quy định thì không ảnh hưởng nhiều đến sức khỏe mà chỉ có mùi hắc rất khó chịu khi sử dụng. Tuy nhiên nếu hàm lượng Clo dư trong nước vượt quá mức cho phép và sử dụng trong thời gian dài sẽ ảnh hưởng không tốt đến sức khỏe chúng ta.
Clo khi tác dụng với các hợp chất hữu có trong nước tạo thành hợp chất THM’s – có thể gây ung thư, trong quá trình sinh hoạt hàng ngày, da chúng ta tiếp xúc với Clo sẽ làm cho da khô và dễ mắc các bệnh ngoài da như ngứa, viêm da…
Ngoài ra tác hại lớn nhất của bom clo chính là gây ra chất độc da cam mà ta đã được chứng kiến biết bao đồng bào đã ngã xuống vì căng bệnh quái ác này. Thậm chí để lại dư chấn cho con cháu họ, ai sinh ra cũng bị khuyết tật, không đầy đặn như người bình thường.
2.- Flo có số oxh duy nhất là -1 mà không có 3, 5, 7 như các halogen khác do nguyên tử F có phân lớp ngoài cùng là 2p. Phân lớp này ko ở gần phân lớp d nào nên ko thể kích thích các e hoá trị ghép đôi sang các obitan d để đạt trạng thái kích thích chứa nhiều e độc thân hơn, do đó chỉ có số oxh 1.
– Các halogen có số oxh lẻ vì ở trạng thái cơ bản, halogen có 1e độc thân. Với Cl, Br I, sau khi kích thích, nó sẽ lên 3, 5, 7e độc thân nên có số oxh lẻ. F tuy ko thể kích thích nhưng có 1e độc thân nên vẫn mang số oxh lẻ.
* Ngộ độc do clo xảy ra khi nuốt hoặc hít phải clo. Clo sẽ phản ứng với nước trong hệ tiêu hoá để hình thành HCl và HClO. Cả 2 chất này đều gây rất độc đối với con người. Các triệu chứng ngộ độc Clo : nóng rát ở miệng, sưng phù họng, nôn mửa, có máu trong phân, tụt huyết áp, tổn thương da,..
*Vì Flo là phi kim mạnh nhất số tất cả các phi kim nên trong phản ứng nó chỉ nhận thêm e nên nó có số oxi hoá âm
– Uống nước có chứa hàm lượng Clo dư quá nhiều có thể gây bệnh hen suyễn, suy giảm hệ miễn dịch và làm giảm chức năng gan. Ngoài ra, Clo là chất có tính tẩy rửa mạnh, vì thế nếu hàm lượng clo trong nước máy cao trên 0,5mg/l có thể gây ảnh hưởng trực tiếp đến da. Với một số người có cơ địa da mỏng thì những ảnh hưởng này có thể thấy được ngay bằng mắt thường chỉ sau một vài lần tiếp xúc và còn gây nhiều bệnh nguy hiểm.
– F là phi kim mạnh nhât nên nó chỉ nhận thêm e -> số oxi hóa âm
-Khí clo gây ảnh hưởng đến đường hô hấp,da, mắt nếu tiếp xúc quá nhiều
-Do F là phi kim mạnh nhất trong các loại phi kim nên trong phản ứng, F chỉ thêm e nên số oxi hoá luôn âm
1/Clo là một chất có thể phản ứng với nước, cả bên ngoài và bên trong cơ thể. Nếu bạn nuốt hoặc hít vào quá mức, chất này sẽ phản ứng với nước trong cơ thể. Phản ứng này sau đó tạo thành axit clohydric và axit hypocloric rất độc đối với con người
+ Tác động lên da:
Clo là chất có tính tẩy rửa mạnh, vì thế nếu hàm lượng clo trong nước máy cao trên 0,5mg/l có thể gây ảnh hưởng trực tiếp đến da. Với một số người có cơ địa da mỏng thì những ảnh hưởng này có thể thấy được ngay bằng mắt thường chỉ sau vài lần tiếp xúc, có thể kể đến như bong da, khô da, dễ bắt nắng, dễ kích ứng với mỹ phẩm (kể cả những loại đã sử dụng quen hay những loại lành tính nhất), dễ mẩn đỏ, ngứa da. Theo thời gian, da của bạn sẽ dần xuất hiện nhiều dấu hiệu của lão hóa như đồi mồi và nếp nhắn.
+ Do nguyên tử F có phân lớp ngoài cùng là 2p. Phân lớp này không ở gần phân lớp d nào nên không thể kích thích các e hóa trị ghép đôi sang cắc obitan d để đạt trạng thái kích thích chứa nhiều e độc thân hơn, do đó chỉ có soh -1
– Nếu bạn vô tình hít phải khí clo, chất này sẽ phản ứng với nước trong cơ thể tạo axit clohidric và axit hypoclodric gây khó thở, sưng họng, phù phổi. Ngoài ra, nó còn làm hỏng hệ tuần hoàn khiến huyết áp thấp, độ PH trong máu mất cân bằng
– Do flo là phi kim mạnh nhất nên trong phản ứng chỉ nhận thêm e. Vì vậy số oxh của nó âm
1.Clo là một chất nguy hại nghiêm trọng đối với cơ thể con người, nó có thể gây kích ứng mắt, mũi, họng và đường hô hấp trên. Nó có thể gây phù phổi cấp và viêm phổi, khi nồng độ cao có thể làm tê liệt trung tâm hô hấp và gây ra tử vong trong chớp nhoáng.
2.Do F là phi kim mạnh nhất nên nó chỉ nhận thêm e vậy nên số oxh luôn âm
Hàm lượng thấp của clo có thể gây nhiễm vi sinh, tiêu chảy đau bụng
Hàm lượng cao gây ngộ độc, khó thở, đau ngực phù phổ
Vì Flo là phi kim mạnh nhất nên trong phản ứng Flo chỉ nhận electron => Luôn có số oxi hóa âm
Một số hậu quả của khí Clo: hàm lượng clo khi vượt quá mức cho phép và sử dụng trong thời gian dài sẽ gây ra các vấn đề về sức khỏe liên quan đến gan, thận hoặc hệ thần kinh, làm tăng nguy cơ mắc bệnh ung thư…
F có số e lớp ngoài cùng của F là 7 (thiếu 1e)-> F là phi kim
Vì thiếu 1e nên phải thêm 1e để được cấu hình bảo hòa (8e)
Do phi kim mang điện âm -> số oxi hóa của F là -1
– Khí clo có màu vàng xanh và có mùi tương tự như thuốc tẩy. Giống như phosgene, nó là một tác nhân gây nghẹt thở, cản trở hô hấp và làm tổn thương các mô trong cơ thể. Clo có thể phản ứng với nước trong niêm mạc của phổi để tạo thành axit clohydric, một chât kích thích có thể làm chết người.
– Ngày 22/4/1915 Quân Đức đã sử dụng Clo để tiêu diệt đối phương trên chiến trường. Khí độc này khiến nạn nhân cảm thấy đau nhói ở cổ họng và ngực.
– Do F là phi kim mạnh nhất nên trong phàn ứng F chỉ nhận thêm e nên luôn có số oxi hóa luôn âm
2/Trong nhóm VIIA,khi đi từ trên xuống dưới tính phi kim giảm dần, Flo là phi kim mạnh nhất và cũng do Flo là nguyên tố đứng đầu halogen nên Flo là phi kim mạnh nhất nên nó có khả năng nhận thêm 1 electron do đó soh của clo là -1
– Clo có thể phản ứng với nước trong niêm mạc của phổi để tạo thành hỗn hợp axit clohydric có thể gây tổn hại lớn đến con người. Phân tử clo lan rất nhanh chóng trong không khí và ở gần mặt đất do nó nặng hơn không khí.
– Do nguyên tử F có phân lớp ngoài cùng là 2p và là phi kim mạnh nhất cho nên nó chỉ nhận thêm e, vì vậy soh là -1
-Tác hại bên ngoài: Nếu da chúng ta thường xuyên tiếp xúc với nước Clo dư thì sẽ có hiện tượng khô da, ngứa viêm da, rát mắt, khô tóc… Đây cũng là những triệu chứng mà chúng ta thường gặp sau khi tắm từ hồ bơi công cộng – nơi có chứa nhiều Clo dư hơn bình thường. Clo càng dư nhiều thì triệu chứng càng nặng nề, gây bong tróc khô da, khô tóc.
-Do Flo là kim loại mạnh nhất nên nó chỉ nhận thêm e=> số oxi hoá âm
Clo gây hử tổn tóc và da, gây hại cho mắt và đường hô hấp.
Giải thích: vì F là phi kim mạnh nhất trong tất cả các phi kim nên trong phản ứng nó chỉ nhận thêm e vậy nên nó luôn luôn có soh là -1.
Clo là chất có tính tẩy rửa mạnh, vì thế nếu hàm lượng clo trong nước máy cao trên 0,5mg/l có thể gây ảnh hưởng trực tiếp đến da. Với một số người có cơ địa da mỏng thì những ảnh hưởng này có thể thấy được ngay bằng mắt thường chỉ sau một vài lần tiếp xúc, có thể kể đến như bong da, khô da, dễ bắt nắng, dễ kích ứng với mỹ phẩm (kể cả những loại đã sử dụng quen hay những loại lành tính nhất), dễ mẩn đỏ và ngứa da.
Trong các hợp chất như NaCl, KCl… Clo thường có mức oxi hóa là -1. Tuy nhiên, clo cũng là một chất có tính khử. Tính khử của clo được thể hiện trong trường hợp tác dụng với Oxi. Các mức oxi hóa của clo thường là +1, +3, +5 hay +7…
*clo là chất tác nhân gây nghẹt thở, cản trở hô hấp và làm tổn hại các mô trong cơ thể. Clo có thể phản ứng với nước trong niêm mạc của phổi để tạo thành axit clohydric, một chất kích thích có thể làm chết người.
*Vì Flo là phi kim mạnh nhất trong số tất cả các phi kim nên trong các phản ứng nó chỉ thu thêm e nên luôn luôn có số oxi hoá âm.Các halogen khác còn có số oxi hoá dương vì còn có những phi kim mạnh hơn chúng nên chúng có thể nhường e cho phi kim này.
– Nếu hàm lượng Clo vượt mức cho phép và sử dụng trong thời gian dài, có thể gây ra các vấn đề về sức khỏe liên quan đến gan, thận hoặc hệ thần kinh. Nó cũng làm gia tăng nguy cơ mắc bệnh ung thư. Ngoài ra Clo còn có thể gây bệnh hen suyễn, rối loạn chức năng gan và thậm chí làm đình trệ và suy yếu khả năng miễn dịch nếu chúng ta uống vào.
– Do F là khi kim mạnh nhất nên nó chỉ nhận thêm e, vì vậy soh là -1
* Ngộ độc do Clo xảy ra khi nuốt hoặc hít phải khí clo. Clo sẽ phản ứng với nước troing hệ tiêu hoá hình thành nên HCL với HClO. Cả 2 chất này đều gây độ đối với con người. Các triệu chứng ngộ độc Clo: Nóng rát ở miệng, sưng phù họng, nôn mửa, có máu trong phân, tuột huyết áp, tổn thương da…
* Vì Flo là phim kim mạnh nhất trong tất cả các phi kim nên trong phản ứng, nó chỉ nhận thêm e, nên số oxi hoá âm.
Tác hại của hàm lượng tồn dư Clo là gì: Uống nước có chứa hàm lượng Clo dư quá nhiều có thể gây bệnh hen suyễn, suy giảm hệ miễn dịch và làm giảm chức năng gan.
Nếu như hàm lượng Clo trong nước máy đạt quá mức tiêu chuẩn đó là trên 0.5 mg/l thì có thể gây ngộ độc cho cơ thể người. Tác động của Clo dư là nhanh hoặc chậm tùy thuộc và độ nhiều và thời gian tiếp xúc của người với Clo trong nước.
Những triệu chứng ban đầu của việc bị ngộ độc bởi Clo dư trong nước như là: ho, khó thở, đau ngực,…Nếu bạn ngửi mùi hắc của Clo quá lâu thì sẽ gây tổn thương cho hệ hô hấp của bạn. Nếu để giác mạc tiếp xúc trong thời gian dài cũng sẽ gây ảnh hưởng xấu. Ở trẻ nhỏ thì điều này càng trở nên nghiêm trọng hơn. Vì Clo là một chất oxy hóa, khi trẻ nhỏ tiếp xúc đặc biệt là trẻ sơ sinh, dù là hàm lượng nhỏ thôi vẫn có thể gây ra hiện tượng sưng tấy cho các tế bào hồng cầu trong máu, làm suy giảm vật liệu trao đổi ion,…
Một điều khá đáng sợ hơn nữa đó chính là Clo có thể tác dụng với một số chất hưu cơ để tạo nên hợp chất THM’S, đây là hợp chất có khả năng gây ra ung thư.
– Số oxh của clo là -1 vì clo là phi kim mạnh nhất nên trong phản ứng nó chỉ nhận thêm e
– Tác hại của clo:
+ Gây ra những bệnh như hen suyễn, rối loạn chức năng gan hay suy yếu hệ miễn dịch. Phụ nữ mang thai sử dụng nước chứa clo có nguy cơ gây sảy thai, dị tật.
– Do lớp e ngoài cùng đã có 7 e nên halogen là những phi kim điển hình, dễ nhận thêm 1e để thể hiện tính oxi hóa mạnh
Tính oxi hóa của các halogen giảm dần khi đi từ F2 đến I2
Trong các hợp chất, F chỉ có mức oxi hóa -1, các halogen khác ngoài mức oxi hóa -1 còn có mức +1, +3, +5, +7
Ngộ độc clo xảy ra khi bạn nuốt hoặc hít phải clo. Clo sẽ phản ứng với nước, bao gồm cả nước trong hệ tiêu hóa, để hình thành axit clohydric (HCl) và axit hypocloric (HClO). Cả hai loại chất này đều rất độc đối với con người.
Ngộ độc clo có thể gây ra các triệu chứng trên toàn cơ thể. Các triệu chứng của hệ hô hấp bao gồm khó thở và hình thành dịch trong phổi. Các triệu chứng ở hệ tiêu hóa bao gồm:
Nóng rát ở miệng
Sưng phù họng
Đau họng
Đau bụng
Nôn mửa
Có máu trong phân
Phơi nhiễm với clo còn có thể gây tổn thương hệ tuần hoàn. Các triệu chứng của hệ tuần hoàn bao gồm:
Sự thay đổi về cân bằng pH trong máu
Tụt huyết áp
Tổn thương mắt nghiêm trọng, bao gồm nóng rát và kích ứng mắt. Trong những trường hợp nhặng nhất, có thể sẽ bị mất thị lực tạm thời
Tổn thương da, có thể để lại hậu quả là tổn thương mô, bỏng và kích ứng da.
– Số oxh của clo là -1 vì clo là phi kim mạnh nhất nên trong phản ứng nó chỉ nhận thêm e
Dạ thưa thầy cho con hỏi là trong tự nhiên, halogen chỉ tồn tại ở dạng hợp chất nhưng vì sao lại có thêm đơn chất halogen vậy ạ
Chào Minh Phước.
🐠Trong tự nhiên, ngoài một lượng rất nhỏ khí Cl2 sinh ra khi núi lửa hoạt động; chlorine (Cl) chỉ được tìm thấy ở dạng hợp chất hóa học – mà phổ biến nhất là NaCl (Sodium chloride – Muối ăn).
🐠Vậy tại sao lại có thêm đơn chất Cl2; nó từ đâu ra vậy?
Câu trả lời là: con người chúng mình đi điều chế lượng nhỏ khí Cl2 (trong phòng thí nghiệm); hoặc sản xuất lượng lớn khí Cl2 (trong công nghiệp).
*Phước xem điều chế Cl2 tại đây (YouTube).
*Phước xem sản xuất Cl2 tại đây (YouTube).
🐠Vậy con người tạo ra khí Cl2 để làm gì?
Câu trả lời là: để dùng trong quá trình sản xuất (cần dùng đến khí Cl2) các hóa chất, dược phẩm, mỹ phẩm, … phục vụ cho cuộc sống con người. Thậm chí trong chiến trang thế giới thứ nhất, người ta còn dùng khí Cl2 là vũ khí hóa học ☣️ để giết người.
*…Cl2 dùng để khử trùng hồ bơi nè, em xem bài viết tại đây nha.
*…Cl2 dùng làm vũ khí hóa học nè Phước.
Còn câu hỏi gì cứ viết lên đây nha Phước.
Chúc em sức khỏe & hạnh phúc,
Trân trọng.