Liên kết hydrogen giữa các phân tử H2O
Chúng mình là các túi NƯỚC biết nói, biết yêu, biết học hỏi và sáng tạo!!! …Liên kết hydrogen giữa các phân tử H2O khiến NƯỚC trở nên vô cùng khác biệt.

Liên kết hydrogen trong túi nước biết yêu ư? Điều đó không hoàn toàn chính xác, nhưng gần đúng vì cơ thể con người có 60 đến 70% là nước. Không chỉ con người, mà hầu hết động vật và thậm chí cả vi khuẩn bé nhỏ cũng được tạo thành chủ yếu từ nước.
Vì sao cơ thể có nhiều nước thế?
Hầu hết quá trình chuyển hóa và hóa học tế bào của sinh vật diễn ra trong “chất nhờn” gốc nước bên trong tế bào của nó, được gọi là bào tương.
Nước không chỉ rất phổ biến trong cơ thể của các sinh vật, mà nó còn có một số khả năng hóa học khác thường để hỗ trợ sự sống rất tốt. Những đặc tính này rất quan trọng đối với sinh học ở nhiều cấp độ khác nhau, từ tế bào đến sinh vật đến hệ sinh thái.
Nước có những đặc tính độc đáo này là do tính phân cực của phân tử H2O; và đặc biệt là khả năng tạo liên kết hydrogen
- giữa các phân tử H2O với nhau (liên kết hydrogen nội phân tử),
- giữa các phân tử H2O với các phân tử khác (liên kết hydrogen liên phân tử).
Dưới đây, chúng ta sẽ xem xét liên kết hydrogen là gì?
Sự phân cực của phân tử H2O
Trong bài Độ âm điện, mình biết do Oxygen có độ âm điện lớn hơn Hydrogen (tức O tham lam điện tử hơn H), nên O kéo rút cặp electron liên kết về phía mình.
Trong bài liên kết cộng hóa trị, chúng mình đã biết phân tử H2O có liên kết cộng hóa trị phân cực (H mang điện dương, còn O mang điện âm). Chúng mình vẽ H2O phẳng lì như sau:

Nhưng vẽ như trên là hổng đúng; do nguyên tử Oxygen, ngoài việc dùng electron hình thành liên kết với 2 nguyên tử Hydrogen, vẫn còn 2 cặp electron. Tất cả các cặp electron (dùng chung và không dùng chung) đều đùn đẩy nhau. Sự đun đẩy này khiến cấu trúc tổng thể của H2O bị uốn cong. Các nhà khoa học xác định được hình dạng đúng của phân tử H2O (gọi là cấu trúc không gian) như sau:
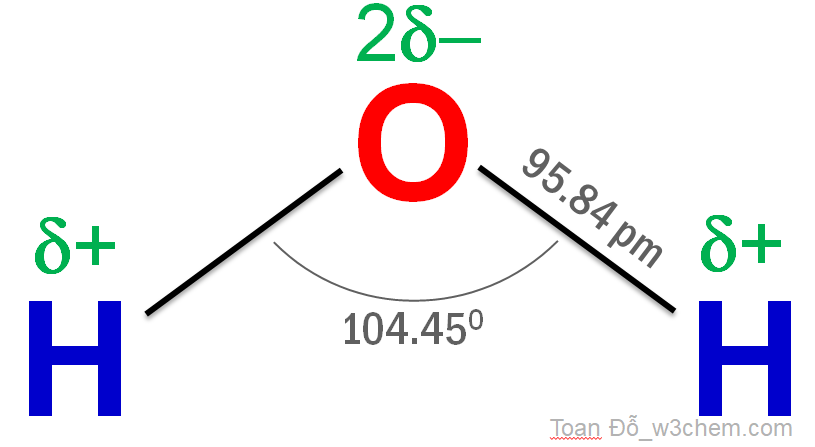
Sự uốn cong phân tử H2O trên được giải thích chính xác hơn bằng sự lai hóa sp3 của O khi tạo liên kết; nhưng cao siêu quá – ta nên bỏ qua. Chỉ cần nhớ: H2O là phân tử phân cực với đầu âm là O; đầu dương là H.
Liên kết hydrogen giữa các phân tử nước
Vẽ liên kết hydrogen
Nhờ sự phân cực, các phân tử nước vui vẻ thu hút lẫn nhau. Đầu H dương của phân tử H2O này bị lôi cuốn và hấp dẫn bởi đầu O âm (gọi là Lực hút tĩnh điện) của phân tử H2O kia. Lực hút tĩnh điện đó:
- được ký hiệu bằng 3 (hoặc nhiều) chấm tròn vo (hoặc gạch đứt ngang – – – – – ; gạch đứng ||||||||||| tùy tài liệu).
- gọi là Liên kết hydrogen.

Giải thích vì sao 1 phân tử H2O tạo được tối đa 4 liên kết hydrogen với 4 phân tử H2O khác? (Bạn hãy trả lời vào phần comment bên dưới).
Tác dụng của liên kết hydrogen
Liên kết hydrogen là liên kết yếu. Hình trên chỉ vẽ vài liên kết hydrogen cơ bản; nhưng ….
… thực tế trong 1 khối nước, có hàng tỷ… tỷ… tỷ… liên kết hydrogen giữa các phân tử H2O và do vậy, lực liên kết hydrogen tăng lên đáng kể. Các nhà khoa học cho biết: nếu không có liên kết hydrogen thì nước sôi chỉ ở – 80 0C thôi!…. khi đó trên Trái Đất hoàn toàn không có 1 giọt nước nào cả – tức sẽ không có sự sống.
Nhờ có liên kết hydrogen mà ở điều kiện thường,
- các phân tử H2O bị “quấn quýt” với nhau, khiến nước ở THỂ LỎNG.
- nước có NHIỆT ĐỘ SÔI CAO đến 100 0C (do cần nhiệt để phá hủy tỷ… tỷ… tỷ… liên kết hydrogen; rồi mới chuyển các phân tử H2O sang thể hơi được).
Nước đá và Nước lỏng khác nhau thế nào?
Ở thể rắn – nước đá có cấu trúc tinh thể phân tử như sau:
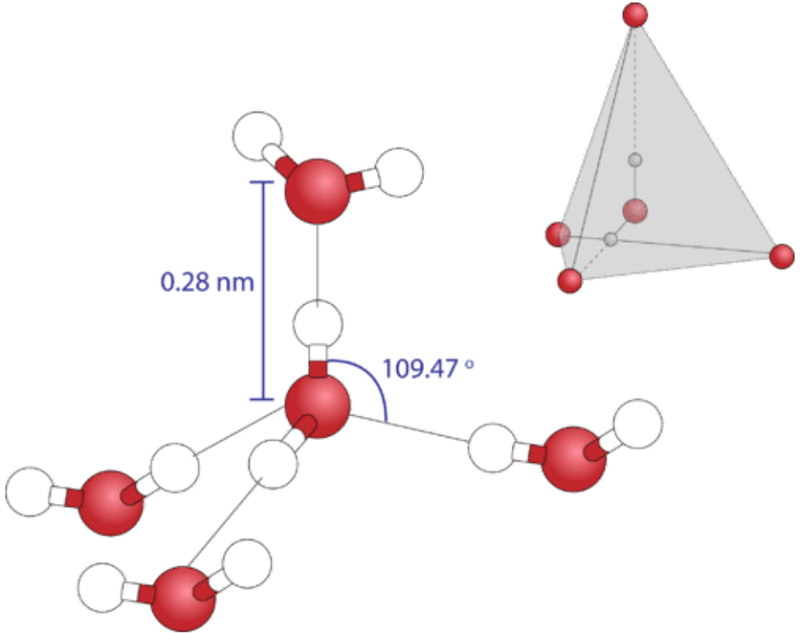
- 4 phân tử H2O nằm ở 4 đỉnh của 1 tứ diện đều – gắn kết với nhau bằng liên kết hydrogen (xem hình vẽ bên dưới; màu đỏ là O, màu trắng là H).
- bên trong tứ diện là khoảng rỗng khiến nước đá “xốp” hơn nước lỏng; do vậy,
- nước đá NHẸ hơn nước lỏng nên nổi được trên mặt nước lỏng.
- cùng 1 khối lượng nước thì Vnước lỏng < Vnước đá.
Không nên để lon bia, nước giải khát (vỏ thủy tinh hoặc kim loại) trong ngăn đá tủ lạnh?
Như trên, mình biết: với cùng 1 lượng nước thì Vnước lỏng < Vnước đá; tức là nước trương nở lên khi đóng băng.
Bia chủ yếu là nước, vậy khi mình đóng băng bia, nước trong bia cũng sẽ nở trương lên. Sự gia tăng thể tích này gây nên áp suất tác dụng lên thành chai (lon) bia. Khi áp suất đủ lớn, chai (lon) bia không chịu nổi nữa – nó sẽ phát nổ.

Điều kiện có Liên kết hydrogen
Bản chất của Liên kết hydrogen là Lực hút đĩnh điện giữa hai phần tử tích điện trái dấu; do vậy …điện tích âm-dương càng lớn thì liên kết này càng mạnh; ngược lại nếu điện tích âm-dương quá nhỏ thì liên kết hydrogen không thể hình thành.
Muốn giá trị điện tích lớn thì H phải gắn với nguyên tử X có độ âm điện lớn do khi đó, X hút mạnh electron của H nên:
- H mất khá nhiều (mật độ) electron (tức mất khá nhiều điện âm) nên tích điện dương lớn.
- X hút được nhiều (mật độ) electron (tức hút nhiều điện âm) nên tích điện âm lớn.
Các nhà hóa học cho biết nguyên tử X là F, O, Cl, N . Do vậy, điều kiện tạo liên kết hydrogen là phân tử có liên kết H—F ; H—O ; H—Cl ; H—N. Khi đó sự tích điện được vẽ đơn giản là
+H—F– ; +H—O– ; +H—Cl– ; +H—N–
Liên kết hydrogen giữa các phân tử NH3 vẽ đơn giản như sau:
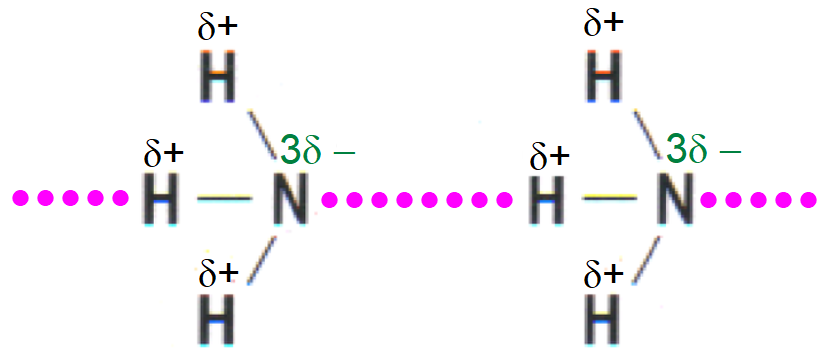
Liên kết hydrogen khiến các phân tử yêu ghét nhau!
Cũng như cuộc sống; trong hóa học, các chất giống nhau thì hòa tan trong nhau. Điều này cũng như chúng mình, nếu tính cách mình giống ai – mình chơi thân với người ấy; còn nhìn mặt thấy ghét – thì thôi nghỉ hổng chơi!
Nước là chất phân cực (có cực dương, cực âm), vì vậy nó cũng tìm kết bạn tâm giao với chất tương tự mình (khi đó cả hai hòa tan vào nhau – các nhà hóa học gọi nước là dung môi phân cực). Các bạn tâm giao của H2O là phân tử:
- có liên kết cộng hóa trị phân cực mạnh giống nước (như NH3, C2H5OH). Sự hòa tan do tạo liên kết hydrogen với nhau.
- có liên kết ion (tồn tại dạng mạng tinh thể ion dương, ion âm như muối ăn – NaCl). Sự hòa tan do lực tương tác tĩnh điện mạnh khiến mạng tinh thể ion bị vỡ bể ra, các ion dương-âm phân ly tan ra.
Sự hòa tan của C2H5OH, NH3 trong H2O do tạo liên kết hydrogen được vẽ như sau:


Sự hòa tan của tinh thể muối ăn được vẽ như sau:

Nước và dầu ăn không ưa nhau!
Vì nước là phân tử phân cực, nó không ưa các phân tử không phân cực như chất béo, xăng-dầu, … Khi mình đổ dầu vào nước, nước ghét dầu nên đẩy dầu ra xa; do dầu nhẹ hơn nước; nên mình thấy dầu nổi lềnh bềnh ở phía trên mặt nước.

Tóm tắt
Nước là một dung môi (phân tử / chất) phân cực.
Một hợp chất phân cực mạnh hoặc hợp chất ion tương tác và hòa tan trong nước được gọi là ưa nước-hydrophilic (hydro có nghĩa là “nước” và philic có nghĩa là “yêu thương”).
Các phân tử không phân cực như dầu, chất béo không tương tác tốt với nước. Chúng tách khỏi nước thay vì hòa tan, được gọi là kỵ nước-hydrophobic (phobic nghĩa là “ám ảnh, sợ hãi”).
Liên kết nhanh
Đọc thêm các bài viết của Hóa lớp 10 tại đây.
Mình là người tự mình thực hiện toàn bộ dự án này – bao gồm xây dựng trang web, viết nội dung, tìm tài liệu tham khảo. Vui lòng xem xét QUYÊN GÓP để hỗ trợ W3chem CHỈ BẰNG CÁCH CHIA SẺ BÀI VIẾT NÀY LÊN MẠNG XÃ HỘI; bởi vì trong tương lai, bạn sẽ cho mình nhiều thời gian để làm việc trên W3chem, cũng có nghĩa bạn có thể nhận thêm nhiều nội dung mới nhanh hơn tại W3chem.
Mình cảm ơn bạn rất nhiều ⤵







