Tính chất hóa học của amine, so sánh tính base các amine
Tính chất hóa học cơ bản nhất của amine là TÍNH BASE (tính nhận ion H+). Hãy cùng tìm hiểu trong bài viết sau bạn nhé.

Cũng như trong cuộc sống, có người cho-người nhận khẩu trang; trong thế giới hóa chất, các phân tử cũng y như vậy. Nhưng bạn nhớ đừng lộn với tính oxi hóa-khử nha (tính cho-nhận electron).
1. Tính base của amine
Ở bài trước, bạn đã biết: trên nguyên tử Nitơ còn 1 cặp electron (mang điện âm); nên amine có khả năng nhận ion H+ ⇔ tính base (theo định nghĩa acid-base đã học ở lớp 11).
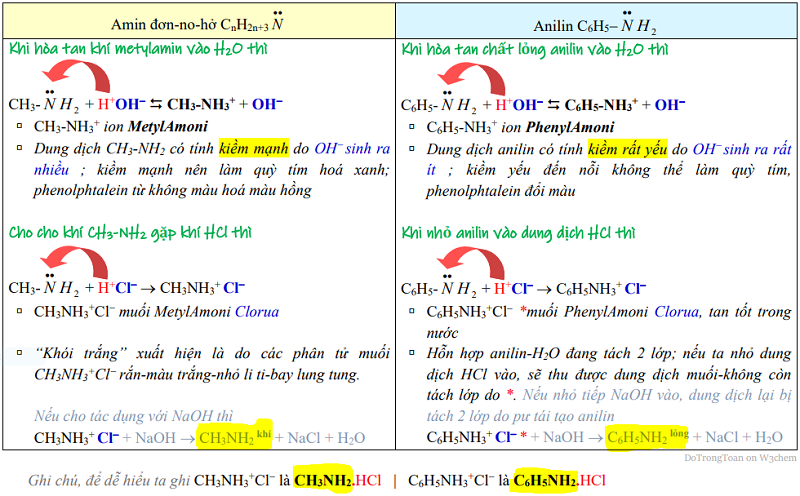
Bạn hãy xem các phương trình nhận H+ của amin đơn-no-hở và anilin theo bảng sau:
Có khi cho viết phương trình với axit khó hơn, nếu thấy rối thì bỏ qua nha bạn!
- CH3NH2 + CH3COOH → CH3COO– CH3NH3+
- 2CH3NH2 + 1H2SO4 → (CH3NH3+)2SO42-
- 1CH3NH2 + 1H2SO4 → CH3NH3+ HSO4–
1.1. Tính base khi cho amine vào dung dịch muối
Tính bazơ của amine cũng thể hiện khi cho phản ứng với dung dịch muối có tạo hydroxide không tan (giống dung dịch NH3 + dung dịch muối). Phản ứng viết ra thấy sợ lắm, ví dụ bạn xem đây:
Dung dịch CH3-NH2 trong H2O ⇔ CH3-NH3+OH– ; Dung dịch C6H5-NH2 trong H2O ⇔ C6H5-NH3+OH. Phản ứng viết là
- (2CH3-NH3+OH–) 2CH3NH2 + 2H2O + Mg2+ → Mg(OH)2 tủa trắng + 2CH3NH3+
- (3CH3-NH3+OH–) 3CH3NH2 + 3H2O + Fe3+ → Fe(OH)3tủa nâu đỏ + 3CH3NH3+
- (2C6H5-NH3+OH–) 2C6H5NH2 + 2H2O + Cu2+ → Cu(OH)2tủa xanh lam + 2C6H5NH3+
Các ion kim loại chuyển tiếp như Cu2+, Zn2+, Ag+, . . . cũng tạo PHỨC chất với NH3, với các amin!
Để đơn giản khi làm toán, mình chỉ cần nhớ như sau là quá đủ
- Ban đầu N: + H2O (H+ OH–) ⇔ NH+ + OH–
- Rồi nOH– + Mn+ → M(OH)n tủa
1.2. So sánh tính base của amine
Ta có bảng so sánh tính base như sau

Gốc RÚT electron (R–<–) của N làm mật độ e (điện tích âm) trên N giảm khả năng hút ion dương H+ giảm ⇔ tính bazơ giảm;
- đương nhiên càng nhiều gốc rút e, tính bazơ càng giảm.
- may quá, chỉ học 1 gốc rút electron là phenyl C6H5-.
Gốc ĐẨY electron (R–>–) vào N có tác dụng ngược lại, làm tính bazơ tăng;
- đương nhiên càng nhiều gốc đẩy e hoặc gốc đẩy e càng mạnh, tính bazơ càng tăng.
- khả năng đẩy e của CH3– < CH3-CH2– < i-propyl (CH3)2CH- < t-butyl (CH3)3C-.
Và còn yếu tố khác ảnh hưởng đến tính base của amine nha, ví dụ như hiệu ứng không gian, gốc R to cồng kềnh, bla …bla …bla.
Ví dụ tính base của
- C6H5-NH2 < NH3 < CH3-NH2 < NaOH.
- (C6H5)2NH < C6H5-NH2 < NH3 < CH3-NH2 < (CH3)2NH < NaOH.
- và còn nhiều bài so sánh hợm hĩnh bạn sẽ gặp ở đâu đó! Hãy cẩn thận.
2. Riêng anilin (nhớ thêm phenol) phản ứng với nước Br2
Anilin C6H5NH2 là chất lỏng không màu ; trong khi phenol C6H5OH là chất rắn màu trắng.
Anilin và Phenol tạo kết tủa màu trắng với nước Br2 ngay ở t0 thường (dùng để phân biệt Anilin và Phenol trong bài tập).

Phương trình phân tử cụ thể như sau:
- C6H5-NH2+ 3Br2 → C6H2Br3(NH2)tủa trắng + 3HBr
- C6H5-OH+ 3Br2 → C6H2Br3(OH)tủa trắng + 3HBr
3. Đốt cháy amine đơn-no-hở
Phản ứng cháy đơn giản lắm, vấn đề là các nhà toán-hóa biến Hóa thành phức tạp, chớ không như là mơ!

4. Một số công thức amine và phản ứng cháy
Các công thức sau khá ghê, bạn cần kiên nhẫn và học với thái độ vui tươi mới đạt hiệu quả! Các công thức này dùng khi cần, nếu thấy khó quá thì nên lướt qua.

Liên kết nhanh
Đọc thêm các bài viết về Amine và Hóa lớp 12 tại đây.
Đừng quên chia sẻ bài viết lên mạng xã hội để nhiều người cùng học nha bạn.








1: alinin hầu như không tan, tạo vẩn đục
2: thu được dung dịch muối không còn tách lớp
3: lại tách thành 2 lớp do tái tạo alinin
Anilin vào nước tạo dung dịch màu đục vì anilin không tan
Nhỏ từ từ HCL vô thì dung dịch đổi màu trong suốt (tạo muối hữu cơ tán)
Nhỏ NaOH vô lại thì dung dịch đục dần do tạo phenyl amin
[1] Dung dịch tách 2 lớp
[2] Thu được dung dịch muối – không còn tách lớp
[3] Dung dịch lại tách 2 lớp do phản ứng tái tạo anilin
1. Anilin ít tan, làm đục dung dịch rồi lắng xuống đáy (tách lớp)
2. Nhỏ dung dịch HCl tới dư vào, anilin tan dần đến trong suốt vì xảy ra phản ứng
3. Tạo lại anilin, làm dung dịch bị vẩn đục như lúc đầu
hiện tượng:
1. Anilin vào nước: nước bị đục, anilin ít tan tách lớp lắng xuống đáy
2. nhỏ HCl vào: anilin tan dần thu được muối, không còn tách lớp
3. nhỏ tiếp NaOH: xuất hiện tách lớp do NaOH tác dụng với muối tạo thành Anilin
Hiện tượng khi:
1) Anilin vào nước tạo dung dịch màu đục vì anilin không tan
2) Nhỏ từ từ HCL vô thì dung dịch đổi màu trong suốt (tạo muối hữu cơ tán)
3) Nhỏ NaOH dô lại thì dung dịch đục dần do tạo phenyl amin
1. Aniline phân thành 2lớp
2. Thu được muối, anilin đồng nhất lại
3. dung dịch lại tách lớp trở lại do phản ứng tái tạo aniline
1. Dung dịch phân lớp.
2. Dung dịch đồng nhất lại.
3. Dung dịch tách lớp trở lại.
[1] Aniline ít tan trong nước làm dung dịch bị đục, để lâu có sự tách lớp.
[2] Aniline tan dần đến trong suốt tạo thành muối phenylamoni clorua tan.
[3] Tạo lại aniline và làm dung dịch bị vẩn đục do tạo phenyl amine
(1) Vì anilin ít tan nên sẽ làm đục dung dịch sau đó lắng xuống -> dung dịch phân lớp
(2) Khi cho HCl vào thì dung dịch đồng nhất trở lại
(3) khi cho NaOH vào thì dung dịch trở lại thành anilin nên tiếp tục phân lớp
(1): Aniline ít tan làm đục dd rồi lắng xuống đáy -> dd bị phân lớp
(2): Nhỏ từ từ HCl vào thì dd đổi màu trong suốt -> dd đồng nhất lại
(3): Nhỏ NaOH thì dd đục dần -> dd tách lớp trở lại
(1) Vì anilin ít tan nên sẽ làm đục dung dịch sau đó lắng xuống -> dung dịch phân lớp
(2) Khi cho HCl vào thì dung dịch đồng nhất trở lại
(3) khi cho NaOH vào thì dung dịch trở lại thành anilin nên tiếp tục phân lớp trở lại
1. Aniline ít tan trong nước tạo dd bị đục, để lâu có sự tách lớp
2.nhỏ từ từ HCl dd đổi màu trong suốt ( tạo muối hưux cơ )
3.nhỏ NaOH dd đục dần ( tạo phenyl amin )
1. Anilin ít tan trong nước tạo dung dịch bị đục.
2. Nhỏ HCl vào Anilin, dung dịch từ đục thành trong suốt, tạo muối hữu cơ
3. Nhỏ NaOH vào dung dịch thì tạo phenyl amine, dung dịch đục dần
Hiện tượng khi cho Aniline vào nước: dung dịch bị vẩn đục
Tiếp tục nhỏ HCl: dung dịch trong suốt
Tiếp tục nhỏ dd NaOH vào: dung dịch vẩn đục trở lại
1, Cho Aniline vào nước
Hiện tượng: Tạo dung dịch màu đục
2, Tiếp tục nhỏ HCl
Hiện tượng: Dung dịch đổi màu trong suốt
3, Tiếp tục nhỏ NaOH
Hiện tượng: Dung dịch đục dần
1. Aniline cho vào nước không tan nên bị đục
2. Nhỏ HCl vào thì dung dịch đổi màu thành trong suốt tạo muối
3. Nhỏ NaOH vào thì lại đục như ban đầu do bị tách 2 lớp tái tạo lại aniline
(1) Aniline vào nước tạo dd màu đục vì aniline không tan
(2) nhỏ từ từ Hcl vào thì dd đổi màu trong suốt
(3) Nhỏ NaOh vào thì dd đục dần do phenyl amin
1) Aniline vào nước tạo dung dịch màu đục vì aniline không tan
2) Tiếp tục nhỏ dd HCL thì dd đổi màu trong suốt
3) Tiếp tục nhỏ dd NaOH thì dung dịch đục dần do tạo phenyl amine
khi cho aniline vào nước thì sẽ có hiện tượng bị vẩn đục do dung dịch phân lớp
tiếp tục nhỏ dung dịch vào hcl vào thì thấy dd đồng nhất lại
tiếp tục nhỏ dung dịch vào naoh vào thì thấy dd tách lớp lại
1. Anilin không tan, làm đục nước rồi lắng xuống đáy
2. Nhỏ dd HCl vào đến khi nước trong suốt tan dần
3. Nhỏ dd NaOH vào, nước bị vấn đục lại
1 Nước bị đục, có sự tách lớp
2 dung dịch đổi màu trong suốt
3. dung dịch đục dần
1. Anilin ít tan, làm đục dung dịch rồi lắng xuống đáy (tách lớp)
2. Nhỏ dung dịch HCl tới dư vào, anilin tan dần đến trong suốt vì xảy ra phản ứng
3. Tạo lại anilin, làm dung dịch bị vẩn đục như lúc đầu
1/ tạo dung dịch màu đục
2/ dung dịch đổi màu trong suốt, dung dịch đồng nhất lại
3/ dung dịch đục dần, dung dịch tách lớp
Aniline ít tan trong nước làm dd bị đục, để lâu có sự tách lớp
Aniline tan dần đền trong suốt tạo thành muối phenylamoni clorua tan
Tạo lại aniline và làm dd bị vấn đục
Hiện tượng khi:
1. Aniline không tan được trong nước
2. Dung dịch trong suốt do tạo muối tan tốt trong nước
3. Dung dịch bị tách 2 lớp do phản ứng tái tạo anilin
1. dung dịch vẩn đục
1) dung dịch phân lớp
2) dung dịch đồng nhất lại
3) dung dịch tách lớp trở lại